Introduction
Le dropéridol, neuroleptique incisif apparenté à l'halopéridol, a été introduit en anesthésie dès sa mise sur le marché, comme composant majeur de la neuroleptanalgésie.
L'évolution des techniques d'anesthésie a peu à peu fait reculer son usage comme agent principal de l'anesthésie, mais l'exploitation de certaines de ses propriétés, en particulier antiémétiques, lui a permis de conserver une place dans la pharmacopée anesthésique.
Par ailleurs, il est largement utilisé pour le contrôle rapide des états d'agitation aiguë de cause psychiatrique.
L'étude de sa pharmacologie reste donc d'actualité, et il garde un intérêt comme adjuvant de l'anesthésie.
En IV:
- Début d'action: 3-10 minutes
- effet de pointe: 30 minutes
- Durée d'effet: 120-240 minutes
Indication
- Prémédication : sédation.
- Prévention et traitement des nausées et vomissements postopératoires.
- Sédation postopératoire.
- Préparation aux examens d’investigation (endoscopie…).
- Agent de neuroleptanalgésie.
- Agent potentialisateur des autres anesthésiques.
Propriétés physicochimiques. Présentation
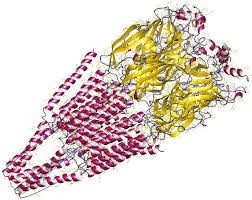
Le dropéridol ou déhydrobenzpéridol est un antipsychotique neuroleptique d'action courte, dérivé de la tétrahydropyridine, de la famille des butyrophénones, décrit par Janssen en 1963.
Le dropéridol est une molécule basique et lipophile.
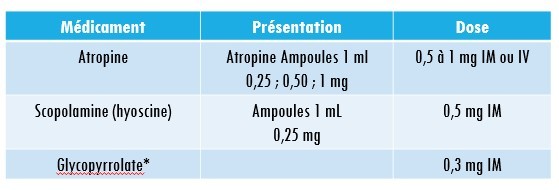
Il se présente en solution injectable à la concentration de 5 mg/ml (Droleptan®, laboratoire Janssen), soit 50 mg par ampoule de 10 ml.
Solution injectable IV à 2,5 mg/ml : Ampoules de 1 ml, boîte de 10.
Les ampoules doivent être conservées à l'abri de la lumière.
Pharmacocinétique
L'absorption du dropéridol par voie intramusculaire de même que par voie orale est rapide (environ 20 et 60 minutes respectivement).
La décroissance de la concentration plasmatique se fait selon un modèle tricompartimental avec une demi-vie d'élimination moyenne de 104 minutes, une clairance d'élimination de 14 ml·kg-1·min-1, ce qui en fait un composé à fort coefficient d'extraction hépatique, et un volume de distribution à l'équilibre de 1,41·kg-1.
Le dropéridol est presque entièrement métabolisé (moins de 1 % de produit natif dans les urines).
Son excrétion biliaire est significative (10 % trouvés dans les fèces).
Sa vitesse d'élimination dépend de la vitesse de retour des compartiments profonds vers le compartiment central.
La cinétique du dropéridol est linéaire dans les zones thérapeutiques habituelles, et indépendante du poids entre 48 et 90 kg et de l'âge entre 14 et 65 ans.
Elle n'explique pas la durée clinique de l'effet (environ 1 heure 30 minutes après une injection intraveineuse directe), ni les effets secondaires retardés.
Il faut pour cela évoquer soit une action prolongée au niveau des récepteurs, soit une rétention intracérébrale du dropéridol.
Propriétés pharmacodynamiques
Son excrétion biliaire est significative (10 % trouvés dans les fèces).
Sa vitesse d'élimination dépend de la vitesse de retour des compartiments profonds vers le compartiment central.
La cinétique du dropéridol est linéaire dans les zones thérapeutiques habituelles, et indépendante du poids entre 48 et 90 kg et de l'âge entre 14 et 65 ans.
Elle n'explique pas la durée clinique de l'effet (environ 1 heure 30 minutes après une injection intraveineuse directe), ni les effets secondaires retardés.
Il faut pour cela évoquer soit une action prolongée au niveau des récepteurs, soit une rétention intracérébrale du dropéridol.
Effets centraux
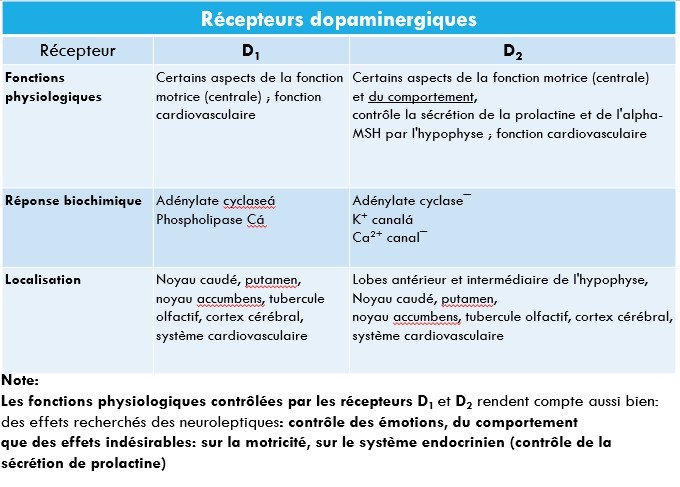
Le dropéridol est un antagoniste des effets des stimulants dopaminergiques.
Ceci explique ses propriétés antipsychotiques.
Il antagonise les vomissements induits par l'apomorphine et révèle des propriétés adrénolytiques.
Des tests chez l'animal ont permis de confirmer que le dropéridol est un neuroleptique puissant et de durée d'action relativement brève .
Comme les autres neuroleptiques, il entraîne chez l'homme les symptômes suivants :
- suppression des mouvements spontanés et du comportement diversifié, tandis que les réflexes médullaires et les attitudes d'évitement de la douleur sont préservés ;
- diminution de l'initiative et perte d'intérêt pour l'environnement ;
- diminution des manifestations d'émotion ou d'affectivité.
L'action sédative et hypnotique du dropéridol est faible, à tel point que l'association de cet agent à des analgésiques centraux puissants permet la réalisation d'anesthésies vigiles, l'opéré restant lucide et coopérant.
Le dropéridol peut induire un syndrome extrapyramidal et cataleptique plus ou moins marqué.
Cet effet indésirable sera décrit plus en détail ultérieurement
Effets cardiovasculaires
A la dose de 0,15 mg/kg IV, le dropéridol induit une diminution marquée de la précharge par augmentation de la capacitance veineuse, qui entraîne une chute de la pression artérielle moyenne sans action sur les résistances vasculaires systémiques.
Les modifications précoces et transitoires observées (augmentation de la fréquence cardiaque et de la contractilité myocardique) peuvent être rattachées à un bref relargage de catécholamines.
Le dropéridol doit être utilisé avec une grande prudence chez le sujet hypovolémique.
Effets respiratoires
Le dropéridol, à la dose de 0,3 mg/kg, n'a pas d'effet dépresseur sur les centres respiratoires .
Il faut remarquer à ce propos que l'index thérapeutique de cet agent est très élevé, et sa toxicité faible.
Effets antiémétiques
Les effets antiémétiques par son action sur les centres dopaminergiques, où il exerce un effet semblable à celui du métoclopramide.
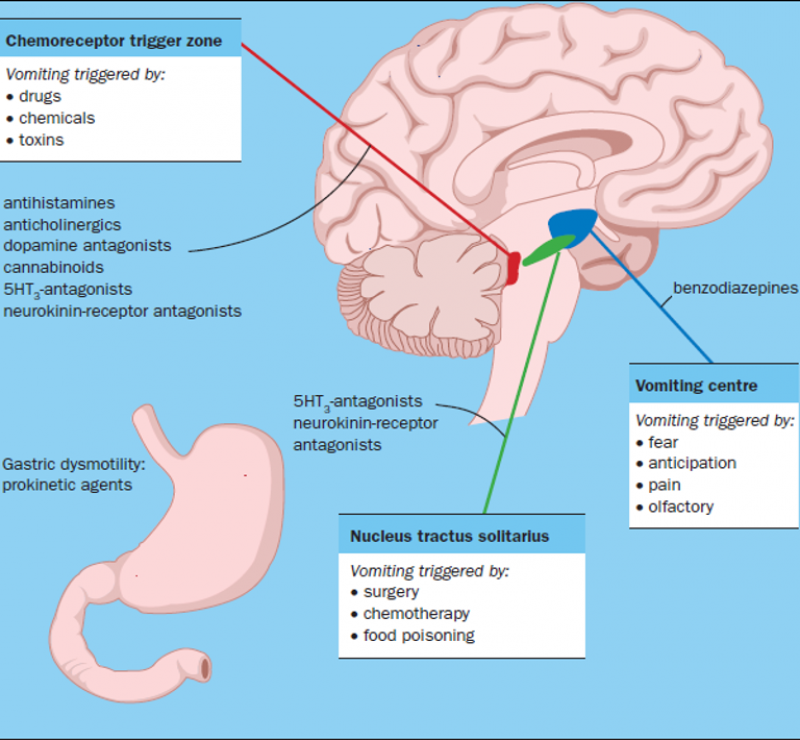
Les NVPO sont déclenchés par la stimulation d'un centre du vomissement situé dans la partie caudale du quatrième ventricule cérébral (partie dorsale de la formation réticulée latérale au niveau du bulbe).
Cette stimulation se fait en partie par l'intermédiaire de l'activation d'une zone " gâchette " (" chemoreceptor trigger zone "), située dans l'area postrema, petite structure en forme de U placée juste en arrière du centre du vomissement.
L'area postrema est située en dehors de la barrière hématoméningée et reçoit aussi bien les stimulations chimiques provenant du sang que du liquide céphalo-rachidien (LCR).
C'est dans cette région que se terminent les afférences vagales et vestibulaires, puissants stimuli émétisants.
Les neuromédiateurs impliqués dans la commande des nausées et vomissements sont la dopamine et la 5-hydroxytryptamine, ce qui explique l'effet antiémétique du dropéridol.
Potentialisation. Synergie d'action
Pas de potentialisation des analgésiques centraux administrés concurremment, mais semble prolonger leur durée d'action (mécanisme inconnu).
Peut être mis à profit dans la période périopératoire pour la prévention par exemple du delirium tremens, ou pour diminuer les doses nécessaires d'agents anesthésiques chez les patients alcooliques chroniques.
L'index thérapeutique élevé permet d'adapter par titration de l'effet les doses nécessaires à chaque patient dans cette indication : ces doses peuvent en effet varier considérablement, de quelques mg à plusieurs dizaines de mg en IVD, ces posologies pouvant être répétées.
Effets divers
Bien que l‘HTM et le syndrome malin des neuroleptiques aient des traits communs, le dropéridol à la concentration de 10 mol·l-1 (en clinique, la concentration dépasse rarement 6 mol·l-1) n'induit pas de contracture sur le muscle squelettique d'homme, et n'augmente pas la contracture induite par l'halothane, la succinylcholine ou la caféine.
Ce fait confirme l'innocuité du dropéridol chez les sujets à risque d‘HTM.
Le frisson POSTOP est responsable d'une augmentation brutale et importante de la consommation d‘O2, parfois difficile à assumer par les patients porteurs d'une cardiopathie.
Le dropéridol diminue la réponse thermorégulatrice et son usage a ainsi pu être proposé pour prévenir la survenue du frisson postopératoire.
Actuellement cependant, l'attitude la plus couramment adoptée est le réchauffement progressif en salle de réveil d'un patient en ventilation contrôlée, ce qui permet d'adapter l'apport d'oxygène à la demande.
Effets secondaires indésirables
Aux doses couramment utilisées en prémédication, le dropéridol peut provoquer des crises dyskinétiques parfois impressionnantes, surtout chez l'enfant.
La fréquence de ce phénomène a été estimée à environ 5 % , et a contribué à la diminution de l'usage du dropéridol comme agent de prémédication. Il est important de noter que ces effets secondaires peuvent être retardés
Le dropéridol, à des doses inférieures à 1 mg/kg, peut également entraîner une akathisie (impossibilité de s'asseoir ou de rester assis) survenant 1 heure 30 minutes environ après l'injection , de même lorsqu'il est associé au métoclopramide.
Le traitement actuel des crises d'akathisie semble être le propranolol, 10 à 15 mg per os, plus efficace que les anticholinergiques.
Utilisation en anesthésie
Prémédication
La principale fonction de la prémédication anesthésique est de minimiser l'anxiété préopératoire, et d'amener en salle d'opération un patient calme et coopérant.
L'indifférence à l'environnement induite par le dropéridol, jointe à un effet hypnotique observé surtout aux doses élevées, en a fait dans les années 1970 un agent de prémédication apprécié.
Comparativement au diazépam, (même un placebo) il et moins hypnotique et beaucoup moins anxiolytique.
Le dropéridol ne semble, par conséquent, pas pouvoir être utilisé seul pour la prémédication anesthésique. Par contre, lorsque l'on recherche une prémédication fortement sédative, comme en chirurgie cardiaque par exemple, son association au midazolam a pu donner toute satisfaction.
Neuroleptanalgésie (NLA)
L'association d'un neuroleptique et d'un morphinique réalise un état de catalepsie associant immobilité et analgésie, décrit dès le début des années 1950 par Huguenard, et repris une dizaine d'années plus tard par De Castro et Mundeleer sous le terme de neuroleptanalgésie.
La combinaison la plus populaire a été le dropéridol associé au fentanyl (combinaison commercialisée dans certains pays sous le nom d'Innovar®), qui assurait une meilleure stabilité hémodynamique et était d'un maniement plus aisé que les " cocktails lytiques ", mélanges de phénothiazines et de morphiniques (mépéridine).
La stabilité hémodynamique induite par la NLA a été contestée, et on a ainsi pu décrire accès hypertensifs et tachycardies.
Ces techniques induisent des dépressions souvent prolongées du SNC, ce qui les a pratiquement fait abandonner
Par contre, leur association au N2o et à des curares a grandement contribué à l'essor de l'anesthésie balancée. Longtemps utilisée sous sa forme pure pour la réalisation de certains examens endoscopiques ou radiologiques, la NLA a progressivement été abondonnée au profit d'associations utilisant des produits de durée d'action plus brève que le dropéridol.
Administration péridurale
L'administration péridurale de dropéridol associé à la morphine réduit la fréquence des effets secondaires induits par celle-ci (NVPO, prurit, hypoTA).
Utilisation dans la prévention des NVPO
A quel moment administrer le dropéridol ?
Le meilleur moment pour administrer le dropéridol dans la prévention des nausées et vomissements postopératoires reste l'objet de controverses.
L'administration précoce, avant ou juste après l'induction de l'anesthésie générale, et en tout cas avant l'incision chirurgicale, est fondée sur l'hypothèse qu'un blocage précoce des récepteurs de la " trigger zone " préviendrait leur activation pendant la chirurgie, et de ce fait diminuerait la fréquence des vomissements postopératoires.
Néanmoins, dans un certain nombre d'études le dropéridol était administré à la fin de la chirurgie avec une efficacité réelle sur la prévention des nausées.
Il peut sembler logique d'administrer un agent dépresseur du système nerveux central plutôt au début qu'à la fin de l'anesthésie, sauf éventuellement lorsque la durée de celle-ci est supérieure à la durée d'action de cet agent, soit environ deux heures.
Quelle est la dose optimale ?
Du fait des effets secondaires du dropéridol, et en particulier de la prolongation du séjour en salle de réveil parfois observée , il semble utile de préciser la dose optimale à administrer pour prévenir nausées et vomissements.
Des doses relativement faibles (0,25 à 2 mg ; 10 à 20 g/kg) sont suffisantes pour prévenir efficacement nausées et vomissements. Il est par conséquent inutile de dépasser ces posologies dans cette indication.
Effets secondaires
L'adjonction de faibles doses de dropéridol (10 à 50 g/kg), à visée antiémétique, au protocole d'anesthésie retarde le réveil et diminue de façon significative les performances psychomotrices évaluées par des tests d'aptitude à la rue.
En anesthésie ambulatoire, cet effet doit être mis en balance avec le temps gagné par la prévention des nausées et vomissements.
Des phénomènes extrapyramidaux et un effet anxiogène ont pu être décrits même aux faibles doses utilisées ici.
Nausées et vomissements induits par la chimiothérapie
Les propriétés antiémétiques du dropéridol ont pu le faire proposer pour le traitement des nausées et des vomissements induits par la chimiothérapie anticancéreuse.
De nos jours, on lui préfère le plus souvent les inhibiteurs de la 5-hydroxytryptamine au niveau des récepteurs S3 (5-HT3), tels l'ondansétron (Zophren®), dont l'efficacité dans cette indication a souligné le rôle majeur de la sérotonine comme neuromédiateur des nausées et vomissements chimio-induits.
Traitement des états d'agitation aiguë
Les propriétés neuroleptiques puissantes du dropéridol (neuroleptique dit incisif), en font un agent de choix du traitement des états d'agitation psychomotrice et d'agressivité .
Les doses nécessaires sont extrêmement variables d'un sujet à l'autre, souvent importantes, de l'ordre de 25 à 100 mg intramusculaires par 24 heures.
Compte tenu des effets hémodynamiques du dropéridol, il convient, avant d'en administrer des doses parfois massives, d'être certain que l'agitation est bien d'origine psychiatrique et ne peut être rapportée à une cause organique, et que par ailleurs le sujet n'est pas hypovolémique (déshydratation aiguë de certains états d'agitation, en particulier le delirium tremens).
INDICATION (Vidal 2020)
- Prévention et traitement des nausées et vomissement postopératoires (NVPO) chez les adultes, et en seconde intention chez les enfants (âgés de 2 à 11 ans) et les adolescents (âgés de 12 à 18 ans).
- Prévention des nausées et vomissements induits par les morphiniques en analgésie auto-contrôlée, en post-opératoire, chez l'adulte (PCA).
POSOLOGIE ET MODE D'ADMINISTRATION (Vidal 2020)
Prévention et traitement des nausées et vomissements post-opératoires (NVPO).
Adultes : 0,625 mg à 1,25 mg (1,25 à 2,5 ml).
Patients âgés (plus de 65 ans) : 0,625 mg (1,25 ml).
Insuffisants rénaux/hépatiques : 0,625 mg (1,25 ml).
Enfants (âgés de 2-11 ans) et adolescents (âgés de 12-18 ans) : de 10 à 50 microgrammes/kg (jusqu'à un maximum de 1,25 mg).
Enfants (âgés de moins de 2 ans) : non recommandé.
En prévention des NVPO, le dropéridol, du fait de ses propriétés anti-émétiques, est indiqué chez les patients présentant un risque modéré à sévère de NVPO. Le risque doit être évalué à l'aide d'échelles ou de scores standards validés, tels que le score simplifié d'Apfel.
Il est recommandé d'administrer le dropéridol 30 minutes avant la fin prévue de la chirurgie. Si nécessaire, l'administration pourra être réitérée toutes les 6 heures.
Chez l'adulte, la prévention des vomissements précoces et des nausées tardives est améliorée par l'administration de doses allant de 0,75 mg à 1,25 mg maximum.
Chez l'adulte et l'enfant, l'administration de doses supérieures s'accompagne d'un risque accru de sédation et de somnolence.
Prévention des nausées et vomissements induits par les morphiniques administrées en analgésie auto-contrôlée, en postopératoire (PCA).
Adultes : 15 à 50 microgrammes par mg de morphine, sans dépasser une dose quotidienne maximale de 5 mg de dropéridol.
Patients âgés (plus de 65 ans) et insuffisants rénaux et hépatiques : aucune donnée n'est disponible.
Enfants (âgés de 2 à 11 ans) et adolescents (âgés de 12 à 18 ans) : le dropéridol n'est pas indiqué dans la PCA.
Chez les patients pouvant présenter un risque d'arythmies ventriculaires, une oxymétrie du pouls doit être effectuée pendant l'administration et pendant les 30 minutes qui suivent une injection intraveineuse unique.
CONTRE-INDICATIONS
- hypersensibilité à la substance active ou à l'un des excipients ;
- hypersensibilité aux butyrophénones ;
- allongement connu ou suspecté de l'intervalle QT (QTc > 450 ms chez les femmes et > 440 ms chez les hommes). Ceci inclut les patients présentant un syndrome du QT long congénital, les patients ayant des antécédents familiaux d'allongement congénital de l'intervalle QT ainsi que les patients traités concomitamment avec des médicaments connus pour leur risque de provoquer des torsades de pointes par allongement de l'intervalle QT (voir rubrique Interactions) ;
- hypokaliémie ou hypomagnésémie ;
- bradycardie (fréquence cardiaque < 55 battements par minute) ;
- traitement concomitant connu pour induire une bradycardie ;
- phéochromocytome ;
- états comateux ;
- maladie de Parkinson ;
- dépression sévère.