Transfusion
LES GROUPE SANGUINS
I) RAPPEL HISTOLOGIQUE ET IMMUNOLOGIQUE :
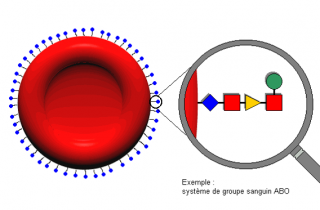
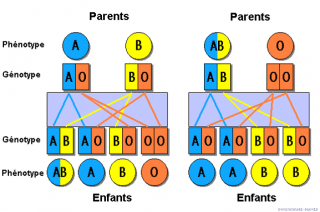
- Il existe dans le système A B O, 4 phénotypes: A, B, AB, O.
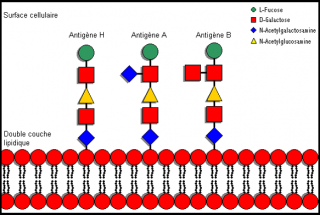
- Groupes sanguins déterminés par les antigènes A, B, H. (déterminés génétiquement et situés sur la paroi des globules rouges).
- déterminés aussi par les anticorps réguliers naturels se trouvant dans le plasma.
le plus important en pratique transfusionnelle
3 antigènes 4 groupes : A, B, AB, O.
Mais…….DANS LE SYSTEME ABO,
IL N’Y A PAS QUE LES ANTIGENES
Particularité du système ABO : présence systématique des ANTICORPS correspondant à (aux) antigènes absent(s)
Groupe A Anticorps anti-B plasmatiques
Groupe B Anticorps anti-A plasmatiques
Groupe O Anticorps anti-A et B plasmatiques
Groupe AB Pas d’anticorps
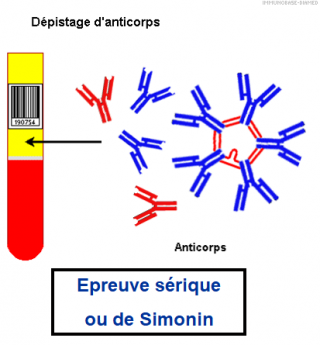
Les anticorps du groupe ABO
ANTICORPS REGULIERS ou NATURELS : base des règles et du danger de la transfusion dans système ABO car anticorps préexistants avant toute transfusion
Origine de ces anticorps : flore intestinale, alimentation. Ce sont des IgM, qui ne passent pas la barrière placentaire.
Apparition dans les 6 premiers mois de la vie.
Le système ABO est doublement défini par les antigènes ET les anticorps.
Une détermination de groupe sanguin dans un laboratoire comporte la recherche des antigènes portés par les globules rouges ET la recherche des anticorps dans la plasma.
| HEMATIES |
PLASMA |
|
|---|---|---|
|
Groupe A |
Antigène A |
Anticorps Anti B |
|
Groupe B |
Antigène B |
Anticorps Anti A |
|
Groupe AB |
Antigène A et B |
Pas d'Anticorps |
|
Groupe O |
Antigène H |
Anticorps Anti A et Anti B |
L'antigène H est le précurseur des antigènes A et B.
Phénotype BAMBAY: présente dans le plasma un anticorps Anti H, il n'a pas d'antigène H, c'est un groupe O.
LE GROUPAGE SANGUIN
|
Epreuve globulaire Hématies patient + sérums-tests |
Epreuve sérique Hématies tests + sérum patient |
||||
|---|---|---|---|---|---|
| Anti-A | Anti-B | Anti-A+B | A1 | B | |
| Phénotype A1/A2 | ++++ | - | ++++ | - | ++++ |
| Phénotype B | - | ++++ | ++++ | ++++ | - |
| Phénotype A1B/A2B | ++++ | ++++ | ++++ | - | - |
| Phénotype O | - | - | - | ++++ | ++++ |
Ces deux épreuves sont indissociables et doivent toujours être cohérentes.
LE SYSTEME ABO : REGLES DE COMPATIBILITE
REGLE FONDAMENTALE :
- Il faut impérativement tenir compte de l’ANTIGENE apporté par les transfusions de concentrés de globules rouges . L’antigène est sur les globules rouges.
- Pour les transfusions de plasma, on tient compte des ANTICORPS . Les anticorps sont dans le plasma.
II ) TECHNIQUES POUR DETERMINER LES GROUPES SANGUINS :
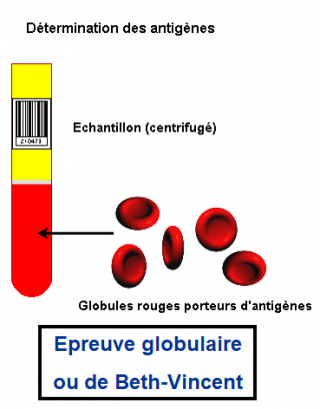
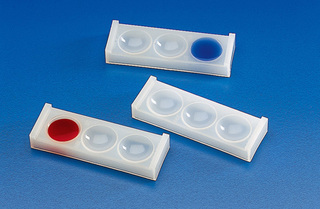
II.1 ) LE BETH-VINCENT :
- Epreuve qui se réalise au CTS et avant la transfusion en contrôle ultime.
- Cette méthode s'effectue avec des sérums test contenant des anticorps connus, afin de mettre en évidence la réaction Antigène - Anticorps.
- La présence ou l'absence d'agglutination permet de déterminer l'Antigène.
La réalisation du contrôle :
II.1.a ) La préparation et la vérification du matériel :
Il faut:
- Une plaque d'opaline ou rhésuscope.

- Une carte de contrôle pré-transfussionnelle.
- Des sérums test Anti A, Anti B, Anti AB: Vérifier la date de péremption et la conservation a + 4°C.
- Un agitateur.
- Un marqueur.
- Des gants.
- Le nécessaire pour essuyer l'agitateur.
- Nécessaire de nettoyage.
II.1.b ) La technique :
- Inscrire sur le support: le nom, prénom, date de naissance du patient, la date du contrôle et le numéro de la poche.
- Inscrire sérum Anti B, Anti A, Anti AB sur la plaque d'opaline.
- Mettre les gants.
- Déposer une gouttes de sérum test.
- Déposer une goutte de sang à coté du sérum test.
- Mélanger et bien essuyer entre chaque utilisation.
- La réaction apparaît une minute après l'agitation.
- Déterminer la groupe en fonction de l'absence ou la présence d'agglutination et vérifier que celui-ci est identique à la carte de groupe du patient et à l'étiquetage de la poche à transfuser.
- Après le passage des culots, nettoyer la plaque, si c'est une carte prè-transfussionnelle la garder sous plastique dans le dossier.
II.1.c ) Détermination du groupe :
|
Anti B |
Anti A |
Anti AB |
Détermination |
|---|---|---|---|
|
Pas de réaction |
Agglutination | Agglutination |
Groupe A |
| Agglutination |
Pas de réaction |
Agglutination |
Groupe B |
|
Agglutination |
Agglutination | Agglutination |
Groupe AB |
|
Pas de réaction |
Pas de réaction |
Pas de réaction |
Groupe O |
II.1.d ) Particularités :
- Patients O dangereux : Ils possèdent des anticorps immuns apparus à la suite de stimulations antigéniques variés (ex: Transfusion, grossesse).
- Les poches étiquetées O dangereux ne peuvent être utilisées que pour des patients du groupe O.
II.2 ) L'EPREUVE DE SIMONIN :
- Dans le système Rhésus il y a D, C, E, c, e.
- Rh+ = Présence de l'Antigène D.
- Rh- = Absence de l'Antigène D.
- Il y a deux techniques de détermination du Rhésus :
- L'une a une température de 37° à l'aide d'un Rhésuscope ( Plaque d'opaline chauffée a 37°) + sérum test Anti D.
- L'autre a température ambiante avec sérum Anti D spécifique dit à froid.
III ) TECHNIQUE POUR DETERMINER LES RHESUS :
III.a ) Réalisation
- Brancher et allumer le rhésuscope.
- Mettre en contact le sérum test Anti D avec une goutte de sang du patient, mélanger avec un agitateur, attendre 2 à 3 minutes et déterminer le rhésus.
III.b ) Détermination :
|
Sérum Anti D |
Détermination |
|---|---|
| Agglutination |
RH+ |
| Pas d'Agglutination |
RH- |
III.c ) Particularités :
- Dans le système rhésus il existe pratiquement pas d'anticorps naturels mais des anticorps immuns.
- L'allo-immunisation est soit transfusionnelle soit foeto-maternelle.
- En France, pour établir une carte transfusionnelle d'un patient il faut deux prélèvements différents, deux techniciens déterminent à l'aide des deux techniques et deux série de réactifs.
IV) LES ACCELERATEURS DE PERFUSIONS.
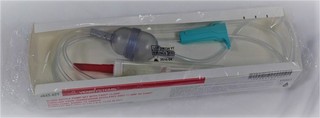
Le transfuseur pour débit rapide
- Il permet la transfusion accélérée de sang et de produits sanguins.
- Comme le transfuseur standard, le transfuseur pour débit rapide ou « blood pump® » comporte un perforateur sans prise d’air, une chambre compte gouttes calibrée avec filtre de 200 microns et une tubulure PVC avec régulateur de débit.
- Il diffère par :
- Le volume important de la chambre compte gouttes qui est de 150 ml.
- La présence, d’une deuxième chambre de 25 ml, en forme de poire, munie d’un dispositif anti-retour à billes.
- Cette chambre permet, par compression manuelle rythmée, l’accélération du débit de la transfusion.
Avantages :
- Installation rapide
- Coût faible (9,24 euros)
- Transport facile donc utilisable en pré-hospitalier
Inconvénients :
- Accélération limitée
- Bien réaliser la purge afin d’éviter l’embolie gazeuse.
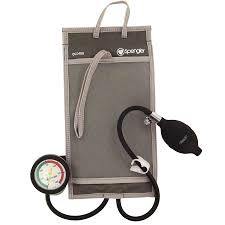
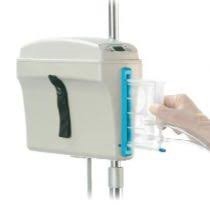
La manchette à pression
Elle permet :
- D’accélérer le débit d’une transfusion en comprimant les poches de sang ou de dérivés sanguins,
- D’accélérer le débit d’une perfusion en comprimant les poches souples d’un soluté de remplissage,
- D’exercer, sur une poche souple de soluté, une contre pression de perfusion d’un cathéter artériel.
- La manchette à pression est une poche en toile inextensible divisée en deux compartiments par un cloisonnement central. Le premier compartiment contient une pochette en caoutchouc gonflable reliée par un tuyau à une poire.
- Cette poire permet une mise en pression ( 0 à 30 cm de Hg) contrôlée par un manomètre.
- Une roulette et une valve assurent le maintien de la pression de gonflage choisie.
- Le deuxième compartiment reçoit la poche à sang ou la poche souple d’un soluté.
- La pression permanente et régulière exercée par le premier compartiment sur le second accélère le débit de la transfusion.
- Il existe deux tailles de manchette à pression : 500 ml et 1000 ml.
Les pompes à galet
- Il s'agit d'un circuit accélérateur de transfusion autorisant un fort débit de perfusion et qui doit être muni d'un détecteur de bulles d'air car le risque majeur de l'utilisation de ce matériel est l'embolie gazeuse.
- De nombreux modèles sont disponibles sur le marché. Son utilisation se fait habituellement avec un réchauffeur de perfusions.
- En général, ce type d'appareil mobilise une personne pour veiller à son bon fonctionnement et aux changements de poches.
- Son mode de fonctionnement est base sur des galets qui entraînent le sang au travers de la tubulure.
uInconvénients :
- Risque d'embolie gazeuse
- Matériel imposant et lourd.
L’utilisation de tels matériaux impliquent généralement des transfusions massives.
Celles-ci impliquent des retentissements a des degrés divers sur l’organisme.
V)LES RETENTISSEMENTS DES TRANSFUSIONS MASSIVES.
Une variation de la kaliémie
- la concentration en potassium des poches de concentrés globulaires augmente proportionnellement à leur durée de conservation.
- Elle atteint en moyenne 30 meq/l vers la troisième semaine.
- L’hyperkaliémie observée lors des transfusions massives est le plus souvent transitoire mais peut devenir préoccupante en cas d’association avec une acidose, ou une anurie.
Une variation de la calcémie
- l’hypocalcémie est la conséquence de la chélation du calcium par le citrate utilisé comme anticoagulant lors du prélèvement.
- Grâce aux nouvelles techniques de séparation du sang, la concentration de citrates est devenue minime dans les culots globulaires.
- Pour leur part, les plasmas frais congelés contiennent une faible quantité de citrates.
- Ainsi, la chélation du calcium par le citrate ne devient gênante que si le métabolisme du citrate est fortement perturbé par des altérations hépatiques.
- L’apport de calcium au cours de la transfusion massive n’est donc plus nécessaire dans la grande majorité des cas.
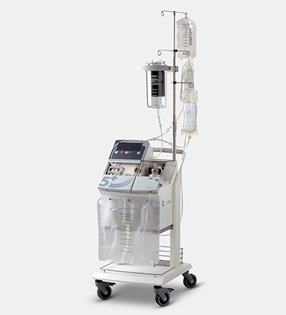
L’hypothermie
- Pour pallier à l’hypothermie et ces conséquences, des systèmes ont vu le jour et cumule l’accélération des transfusions tout en réchauffant les culots qui sont en train de passer. C’est le cas du Level One®
VI)LES RECHAUFFEURS A TRANSFUSION.
- Il existe trois types de réchauffeur.
- A chaleur Humide
- A chaleur sèche
- A double courant
- Pour que le réchauffage d’un soluté soit optimal ,il faut que la déperdition de chaleur soit minimale.
- Par conséquent la ligne de réchauffage sera branché au plus pré du patient.
Le réchauffeur à chaleur humide.
- De type Hot Line
- Tubulure à serpentin plongé dans un bain marie à 37° C
- Circulation d’eau tout au long de la ligne de perfusion.
- Administration de solutés normothermiques et de sang à des débits modérés.
Le réchauffeur à chaleur sèche.
- Type Medi Temp 2®
- Tubulure spécifique composée d’une cassette souple, qui, introduite dans l’appareil est réchauffée grâce à un produit spécifique.
- L’appareil ne commande pas le débit.
- La tubulure est longue et moulée dans un sac en matière plastique maintenu entre 2 plaques chauffantes.
- Un piège à bulle est situé au niveau de la tubulure.
- Le réchauffage des solutés se fait a 43 °C. Il sera débit dépendant.
Le réchauffeur à double courant.
- Type Level One®
- Réchauffement dans un échangeur thermique en aluminium par un bain d’eau chaude circulant à contre courant.
- Tubulure gainée pour permettre un réchauffement continu
- Double système déchange associant réchauffement et accélération.
VII)LES ECHANGES PLASMATIQUES.
- La plasmaphérèse a pour but d’effectuer un échange du plasma du malade par un autre plasma.
- Cette technique est utilisée chez les malades possédant dans leur sang des éléments toxiques ( comme des protéines, des anticorps,certains lipides etc…) qui sont à l’origine de sa maladie.
- Souvent associées aux immunoglobulines intraveineuses, les échanges plasmatiques ont pour but de déprimer le système immunitaire.
- La compensation du plasma extrait peut être réalisée avec de l’albumine à 4%.
- Une partie de la compensation peut comporter des colloïdes de synthèse (amidons).
- Le PFC n’est utilisé que pour traiter le purpura thrombotique thrombocytopénique ou lorsqu’il existe un risque hémorragique important.
- Le PTT (purpura thrombotique thrombocytopénique (PTT) ou maladie de Moschcowitz) associe à des degrés divers une hémolyse intravasculaire avec thrombopénie, une atteinte neurologique et une atteinte rénale.
- Il existe des formes de passage entre le syndrome hémolytique et urémique initialement décrit chez l’enfant et le PTT décrit chez l’adulte.
- La physiopathologie est mal connue, mais il apparaît qu’il existe un déficit de facteurs stabilisant de la prostacycline et présence en circulation d’un facteur agrégant plaquettaire.
- Dans cette indication l’EP permet de perfuser d’importants volumes de plasma.
- La comparaison d’un traitement par échanges à un traitement par du PFC sans échanges fait apparaître une amélioration du pronostic grâce aux E.P.
VIII) LES ECONOMIES DE PRODUITS SANGUINS.
Le prélèvement autologue.
- La transfusion autologue programmée (TAP) consiste à transfuser au patient son propre sang à l’occasion d’une intervention programmée présentant un risque hémorragique. Elle permet de faire une réserve de sang du malade et stimule son érythropoïèse.
- Le prélèvement autologue, qui débute habituellement 4-5 semaines avant l’intervention, diminue nettement les besoins de transfusion homologue, ou les quantités transfusées.
- La durée de la période de prélèvement préopératoire est limitée par la durée de conservation du sang, en général 35 jours.
- Si les globules sont congelés, la période de prélèvement peut être presque indéfiniment prolongée.
- Les banques de sang recommandent de n’effectuer les prélèvements que si l’hémoglobinémie est au moins à 11 g/dL, de laisser un laps de temps minimal de 3 jours entre chaque prélèvement et de ne pas prélever dans les 72 heures précédant l’intervention.
- Sachant que la quantité prélevée ne doit pas dépasser 10 ml/kg lorsqu’il n’y a pas de compensation volémique et 12 ml/kg en cas de compensation volémique.
- Dans les cardiopathies, certains centres perfusent des cristalloïdes lors du prélèvement pour maintenir la normovolémie.
- Le prélèvement autologue doit être évité en cas de rétrécissement aortique sévère et dans l’angor instable.
- Le TAP est rarement utilisée au dessous d’un poids de 15-20 kg en raison des difficultés d’abord veineux.
L’hémodilution normovolémique.
- C’est un acte comportant un prélèvement délibéré de sang effectué en vue de sa transfusion per opératoire.
- Le volume sanguin prélevé est simultanément compensé par un produit de remplissage vasculaire en quantité suffisante pour maintenir la volémie normale.
- L’hémodilution normovolémique réalisée avant les pertes sanguines peropératoires permet de disposer de sang frais autologue pour une transfusion ultérieure.
- De plus, si on effectue une hémodilution jusqu'à obtenir un hématocrite de 30% ou moins, toute hémorragie per opératoire fera perdre plus de plasma et moins de globules rouges.
- Le sang prélevé est ré administré au patient une fois l’hémorragie contrôlée.
- Bien évidemment, si l’hémorragie est massive, le sang frais autologue doit être transfusé avant tout sang homologue.
- Il faut aussi tenir compte du fait que l’hématocrite est de 70-80% environ.
- L’hémodilution seule ne permettant pas toujours d’éviter une transfusion homologue, il peut être particulièrement utile de l’associer à des prélèvements autologues préopératoires.
- L’hémodilution est aussi très utile en cas de dysfonctionnement plaquettaire per opératoire (CEC), puisque le sang prélevé contient des plaquettes normales et des facteurs de la coagulation.
Condition pour l’hémodilution normovolémique.
- Le prélèvement sanguin pour un adulte doit être au moins égal à 500 ml ;
- Pendant le prélèvement, la normovolémie doit être maintenue par des solutés de remplissage en quantité suffisante.
- Le taux d’hématocrite à la fin du prélèvement doit être inférieur à 32% ;
- Les poches de recueil du sang autologue sont étiquetées au nom du patient et conservées dans la salle d’opération ;
- La transfusion des poches réalisée après contrôle ultime ABO pré transfusionnel ;
- Le délai entre le prélèvement sanguin et la transfusion ne doit pas excéder 6 heures ;
- Les poches non transfusées doivent être détruites par l’ES ; cette information doit figurer dans le dossier transfusionnel du patient ;
- Le contrôle de qualité des prélèvements comprend : le dosage de l’hémoglobine libre, la mesure de l’hématocrite et la mise en culture bactériologique.
IX)LA RECUPERATION DE SANG PER-OPERATOIRE.
Qu’est ce qu’une intervention chirurgicale hémorragique ?
- Une intervention chirurgicale est considérée comme hémorragique lorsqu’elle est associée à la nécessité de transfuser le patient pour maintenir une homéostasie de bonne qualité.
Le volume de sang épanché en péri opératoire peut varier en fonction :
- Du type de chirurgie ( cardiaque, vasculaire, orthopédique),
- De la technique opératoire et s’il s’agit d’une intervention de première intention ou d’une reprise chirurgicale ( les reprises chirurgicales étant plus hémorragiques que les interventions de première intention),
- De la pratique du chirurgien, de la qualité de l’hémostase pratiquée par celui-ci,
- De la pathologie responsable,
- Du type d’anesthésie,
- Du degré d’hypothermie induite chez le patient ( chirurgie cardiaque),
- Du traitement anticoagulant du patient ainsi que des éventuels traitements associés.
Quelques données
- Volumes de sang épanché en peropératoire
- 123 à 1172 ml => prothèse de hanche.
- 100 à 3631 ml => chirurgie du rachis.
- 155 à 3200 ml => cardio-vasculaire.
- 125 à 1500 ml => obstétricale.
- Volume de sang épanché en postopératoire
- 315 à 929 ml => prothèse de hanche.
- 112 à 1125 ml => rachis.
- 220 à 4340 => prothèse de genou.
- 1463 à 2763 ml => cardio vasculaire.
- Volume de sang épanché en traumatologie
- 280 à 6000 ml => hémothorax.
- 500 à 4000 ml => hémopéritoines.
Modalités
Les pertes hémorragiques sont recueillies par drainage d’une cavité corporelle ou d’un espace articulaire ou par aspiration dans le champs opératoire. Le sang récupéré est :
- Soit collecté dans un dispositif adapté à usage unique, permettant une transfusion directe après filtration.
- Soit traité avant retransfusion, dans un système qui permet de concentrer et de laver les hématies récupérées.
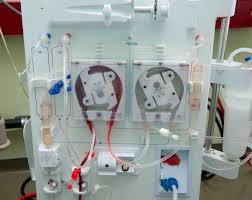
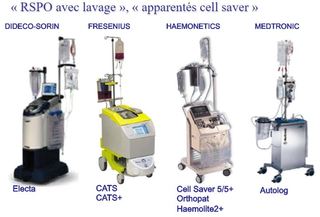
X) LES RECUPERATEURS DE SANG AVEC LAVAGE..
Principe de fonctionnement.
- Les récupérateurs de sang avec lavage dérivent des séparateurs de cellules utilisés dans l’aphérèse, qu’elle soit thérapeutique ou pour transfusion homologue.
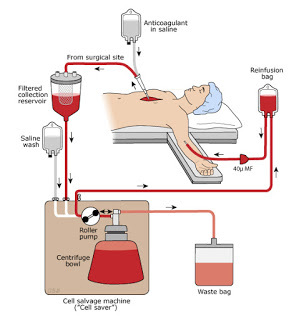
- Ils permettent de réaliser le recueil de sang épanché et son traitement avant qu’il ne soit administré par voie IV.
- Le cycle de traitement est commun à tous les appareils et consiste en une concentration des éléments figurés du sang par centrifugation, un lavage des globules rouges, une élimination du plasma, des leucocytes et des plaquettes dans le surnageant.
- Selon les modèles de récupérateurs de sang avec lavage commercialisés en 2005 sur le territoire français, le lavage peut être continu ou séquentiel, la centrifugation s’effectue dans un bol, un anneau ou un disque dynamique.
La récupération du sang épanché.
- La récupération du sang épanché s’effectue au niveau du champ opératoire par l’intermédiaire d’un dispositif médical à usage unique (DMU) composé des éléments suivants :
- Une prise de vide, la pression d’aspiration pouvant être réglée à l’aide d’un manomètre entre -80 et – 300 mm gH
- Une ligne d’aspiration chirurgicale couplée à une ligne d’anticoagulation (selon les données des fournisseurs : héparine à la concentration de 3000 U / I de sang épanché récupéré) ;
- Un réservoir de recueil du sang épanché de capacité comprise entre 2 et 5 litres et muni d’un filtre de 40 ou 120 microns.
- L’ensemble sang épanché récupéré + anticoagulant est stocké après filtration dans le réservoir de recueil.
Le traitement du sang épanché récupéré.
- L’objectif du cycle de centrifugation lavage vidange est double :
- Obtenir un produit sanguin RSPO ayant un hématocrite compris entre 50 et 70% ;
- Eliminer les produits endogènes et exogènes aspirés en même temps que le sang épanché
- Produits endogènes : hémoglobine libre, PDF, D-dimères, facteurs de la coagulation activés, débris cellulaires, agrégats fibrino plaquettaires , particules osseuses, particules lipidiques.
- Produits exogènes : particules métalliques
- La partie traitement du sang épanché récupéré est assurée par l’intermédiaire d’un appareil et d’un DMU composé des éléments suivants :
- Une pompe ( vitesse de 0 à 1000 ml/min) qui permet de transférer le contenu du réservoir de recueil dans le bol de centrifugation, l’anneau ou le disque dynamique ;
- Un bol de centrifugation, anneau ou disque dynamique qui a une capacité comprise entre 100 et 250 ml ( les bols pédiatriques ont une capacité de 55- 70 ml)
- Une centrifugeuse dont la vitesse de rotation est comprise entre 2,5 et 10 litres ;
- Une poche de stockage du produit sanguin RSPO de capacité comprise entre 400 et 1000 ml ;
- Des lignes assurant la connexion des différents éléments.
- Le temps nécessaire au traitement du volume de sang épanché récupéré dans le bol de centrifugation est conditionné par
- la valeur de son hématocrite,
- le volume du bol,
- le débit de remplissage,
- le volume de la solution de lavage
- et le débit de lavage.
- La durée pour un cycle standard de centrifugation lavage vidange est de 5 minutes.
- Dans ces conditions, les appareils peuvent traiter un volume de 1-2 litres de sang épanché récupéré par heure.
Etape n° 1 : Séparation des éléments figurés du sang épanché récupéré
- Les composants sanguins soumis à la force centrifuge migrent en fonction de leur densité, les plus denses s’éloignant de l’axe de rotation ( densité du plasma < densité des plaquettes < densité des globules blancs < densité des globules rouges).
- Lorsque le bol de centrifugation, l’anneau ou le disque dynamique est plein (détecteur de niveau) surnageant est éliminé dans une poche à déchets.
- L’hématocrite du produit sanguin RSPO présent dans le bol augmente au fur et à mesure que le sang épanché pénètre dans ce dernier et que le surnageant est éliminé dans la poche à déchets.
Etape n° 2 : lavage
- La solution de lavage utilisée est du sérum physiologique isotonique (conditionné en poches homologuée pour injection intraveineuse) dont le volume a été prédéfini par le fabricant.
- Le lavage en continu permet de traiter le sang épanché récupéré (centrifugation lavage vidange) en une seule phase, sans temps d’arrêt pour le remplissage ou la vidange du bol de centrifugation.
- Le lavage séquentiel inclut des temps d’arrêt entre chacune des phases du cycle, au moment du remplissage et de la vidange du bol de centrifugation ; il nécessite qu’un volume minimal ( 45- 800 ml selon les modèles) soit présent dans le réservoir de recueil pour que le cycle de traitement débute en mode automatique.
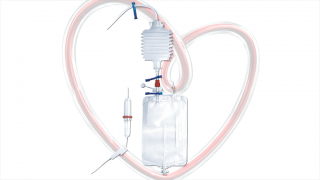
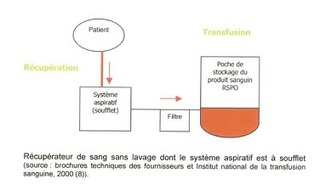
Descriptif et principe de fonctionnement.
Principe de fonctionnement.
- Les récupérateurs de sang sans lavage dérivent des dispositifs utilisés en peropératoire pour récupérer le sang épanché au niveau du médiastin lors des chirurgies cardiothoraciques.
- Ils associent la fonction drainage filtration et la fonction récupération de sang épanché au niveau d’une cavité articulaire (chirurgie orthopédique), pleurale( hémothorax ) ou médiastinale (chirurgie cardiothoracique).
- Ils sont en 2005, principalement utilisés en postopératoire, au cours duquel le sang épanché est aspiré, filtré et stocké avant d’être administré au patient.
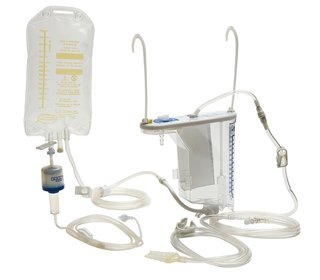
Descriptif technique
- Les récupérateurs de sang sans lavage sont des dispositifs stériles à usage unique qui comprennent :
- une tubulure de drainage,
- un ou plusieurs réservoirs de recueil,
- un système d’aspiration,
- une poche de stockage du produit sanguin RSPO non lavé,
- une tubulure de perfusion,
- un ou plusieurs filtres
Préfiltration :
- Une préfiltration du sang épanché récupéré est réalisée au niveau de la tubulure de drainage en amont du réservoir de recueil via un filtre ( 40, 80, 120 ou 200 microns selon le dispositif).
Aspiration
- Le système d’aspiration est variable selon le dispositif et le fournisseur :
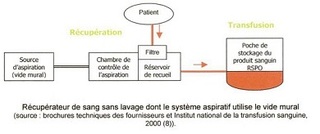
- il utilise soit le vide mural,
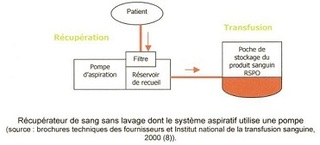
- soit une pompe munie d’une valve anti retour,
- soit un soufflet manuel muni de valves anti retour.
- La régulation de la pression d’aspiration ( 25-160 mm Hg selon les dispositifs) se fait à l’aide soit d’un manodétendeur à membrane, soit d’un manomètre à eau.
Recueil de sang épanché.
- Le sang épanché est récupéré dans un réservoir de recueil qui peut être souple ou rigide et de contenance variable ( 500 à 3290 ml) selon le dispositif.
- Deux types de dispositifs sont disponibles : l’un incluant un réservoir de recueil (qui peut être à une ou plusieurs chambres) et une poche de stockage du produit sanguin RSPO non lavé ; l’autre dans lequel le réservoir de recueil fait également fonction de poche de stockage.
- Certains dispositifs comportent un système de rétention du surnageant qui contient les particules lipidiques pouvant être présentes dans le sang drainé.
XI) LES ALTERNATIVES A LA TRANSFUSION.
Les hémoglobines modifiées substituts des globules rouges.
- L'hémopure® récemment approuvé par la fédération américaine des aliments et drogues (FDA), contient de l’hémoglobine purifiée, retirée du sang d’un bœuf et ne présentant pas, autour des globules, de membrane pouvant être à l’origine des réactions de rejet lors de la transfusion.
- Diaspirin Crosslinked Hemoglobin » ou DCLHb: hémoglobines modifiées
L’erythropoïétine
- L’érythropoïétine est une hormone naturelle glycoprotéique produite par le rein qui agit exclusivement sur les cellules de la lignée érythoïde
- La dose de 100 Ui/kg d’Epo administrée 4 fois par semaine en sous cutanée pendant 4 semaines apparaît plus efficace dans l’augmentation de la réponse des réticulocytes et des valeurs d’hématocrite de départ.
La thrombopoïétine.
- La thrombopoïétine est une protéine qui stimule la production de plaquettes sanguines
Le fer intraveineux.
- L’administration intraveineuse est très efficace sur le plan de la libération et de l’utilisation du fer.
- 80% du fer plasmatique, en continuel renouvellement sont destinés à la moelle érythropoïétique.
- La demi-vie du fer dans le plasma est de quelques heures.
- Le fer intraveineux existe sous deux formes :
- la première est un complexe d’hydroxyde ferrique avec du dextran ( complexe fer dextran) effets secondaires nombreux ( choc anaphylactique, hypotension, bronchospasme, fièvre, convulsion..)
- et un complexe d’hydroxyde de fer trivalentsaccharose ( venofer® ) dépourvue d’effets secondaires
BIBLIOGRAPHIE.
(1) Réanimation et Urgences, collection Abrégé Connaissances et Pratiques, sous l’égide du Collège National des Enseignants de Réanimation Médicale, édition Masson, pages 113-117.
(2) Traité d’Anesthésie Générale, Bernard Dalens, Edition Arnette, page 1571.
(3) Les matériels et les techniques de réanimation pré-hospitalière. Les UMH des SAMU, SFEM Editions collection Médecine d’Urgence SAMU, pages 52-53.
(4) Manuel d’Anesthésie Clinique, Protocoles du Massachusetts General Hospital, 2eme édition, éditions Pradel, pages 565-566.
(5) Le guide de l’infirmière en salle de réveil, éditions Lamarre, pages 195-203.
(6) Echanges Plasmatiques en réanimation, Conférences d’actualisation 1996 Elsevier, pages 533-542.
(7) Récupération de sang périopératoire suivie de son administration par voie intraveineuse, Haute Autorité de Santé, Service évaluation médicoéconomique juillet 2006, pages 5-120.
(8) Récupération de sang en SSPI, Dr C. Deneux et O.Neuville, Jlar 2002.
(9) Les alternatives à la transfusion, Association Nordiste des Infirmier(e)s Anesthésistes Diplomé(e)s d’Etat,B Remy 1998 ,pages 2-4.
(10) Le fer intraveineux en pratique, applications cliniques, éditions Therabel Lucien Pharma, pages 42-45.
Date de dernière mise à jour : 28/02/2020
Ajouter un commentaire