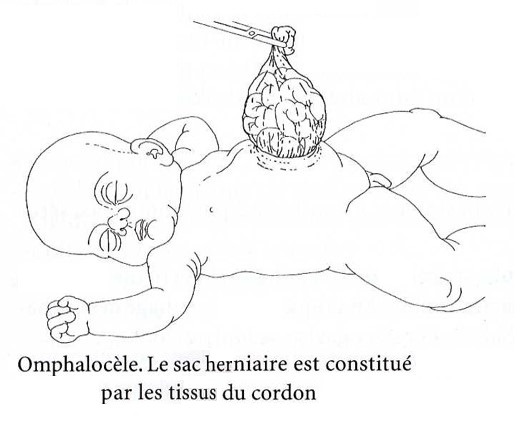
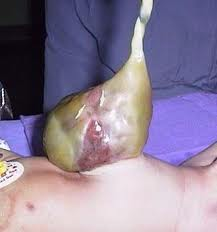
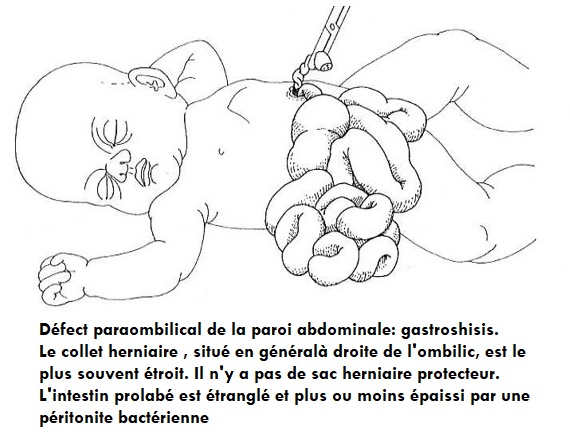
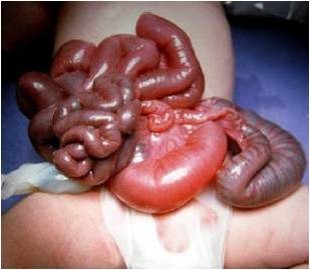
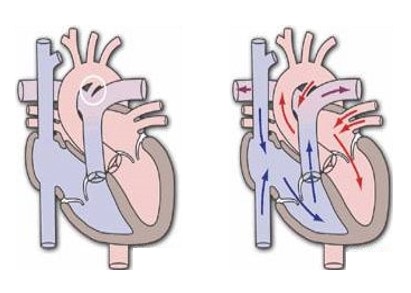
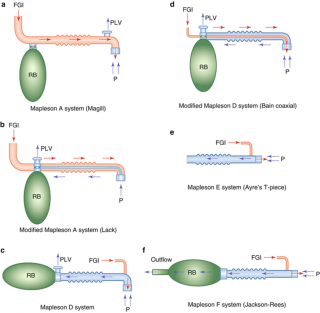
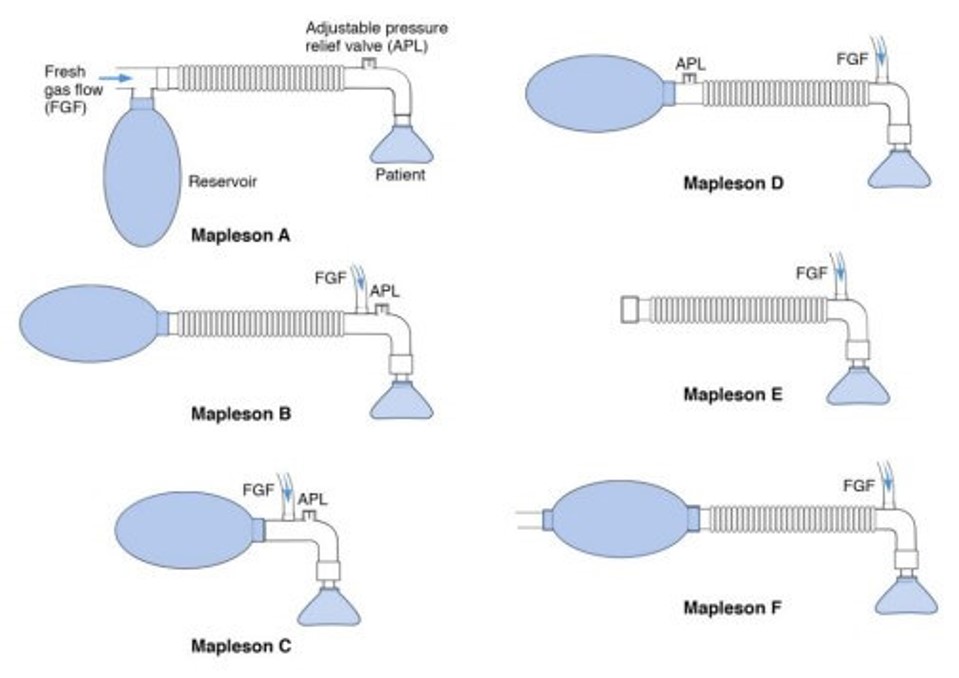
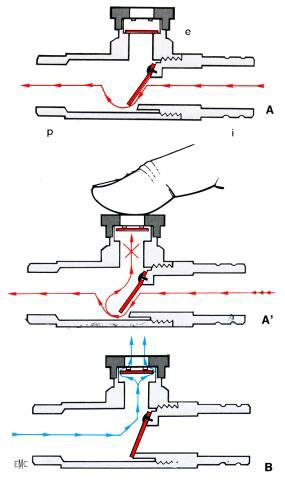
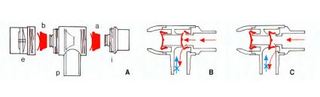
La taille du problème
- arrêts cardio-circulatoires :19/ 10000 avant 1 an 1/10000 de 1 à 14 ans
- prépondérance masculine(65%)
- AG => (89%) des accidents
- morbidité des hypoxies per op plus sévère en pédiatrie
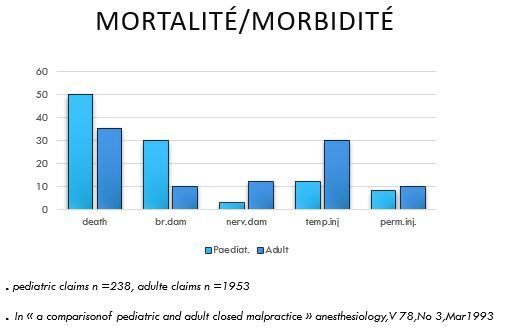

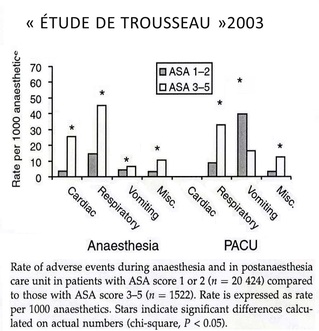
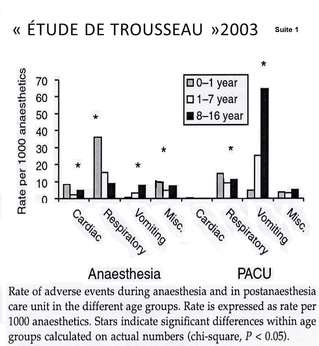
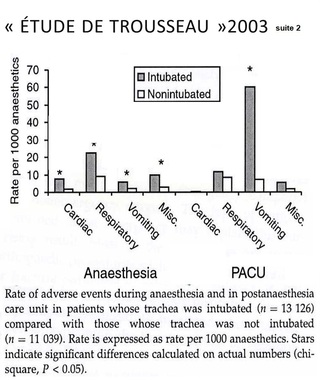
Les facteurs
- Les enfants de moins de 1 an (70% des ACC) la majorité des enfants sont ASA1 ou 2(# de l ’adulte)
- Le statut ASA : facteur prédictif
- L ’anesthésie générale (80%) >AG+AL ou AL seule (1 et 9%)
- L’urgence de l ’acte : taux de morbidité 4 fois supérieur par rapport à l ’activité programmée
LA PRATIQUE OCCASIONNELLE DE LA PEDIATRIE ⇒ RISQUE X 20 ( pour 10000 enfants)
- 70% des ACC iatrogène => médicamenteuse cardiovasculaire
- Evolution dans le temps :
- 1975 égale proportion des causes cardiovasculaires et ventilatoires
- 1985 causes ventilatoires prédominantes sur les causes cardiologiques ou surdosage en anesthésiques
- Halothane => Première cause sur enfant ASA 1
Tout ACR est respiratoire jusqu'a preuve du contraire => Erreur humaine => 90%des causes
Préparation : facteur essentiel de la sécurité
- Vérification du matériel d ’anesthésie et du monitorage
- Préparation des drogues anesthésiques
avant l’arrivée de l’enfant en salle
- Voie veineuse purgée de toutes bulles
- Contrôle d ’identité(par le bracelet nominatif)
- Autorisation parentale datée et signée
Consultation d'anesthésie
Attention toute particulière pour les VASup.
Notés le poids et la taille. Car si cassure de la croissance staturopondérale⇒ début d'une affection sévère.
L'examen de la sphère ORL doit être soigneux :
- hypertrophie amygdalienne,
- dents branlantes ou manquantes,
- appareil dentaire fixe ou amovible.
Recherche des critères prédictifs d'intubation difficile par trois tests :
- ouverture de la bouche,
- extension de la tête,
- mesure de la distance thyromentale.
Cardiovasculaire:
comparer les valeurs de la FC et de la PA / valeurs normales pour l'âge (TA chez enfant qui pleure et agité est sans valeur)
Recherche d’un souffle organique et fonctionnel apprécié par un examen simple comprenant quatre étapes :
- compter la fréquence cardiaque ;
- regarder la coloration des ongles, des lèvres et de la peau ;
- apprécier l'impulsion précordiale ;
- évaluer l'amplitude des pouls périphériques au niveau des bras et des jambes .
Si une anomalie est suspectée, un examen plus complet est indiqué et l'enfant est alors adressé à un cardiologue pédiatre.
La cyanose doit être affirmer par la SaO2 à l'oxymètre de pouls.
Induction
Préparation
La préparation de la salle est un facteur essentiel de sécurité .
Vérification
- du matériel d’induction (adapté à l’âge et au poids de l’enfant).
- du monitorage,
- préparation des drogues anesthésiques avant l’arrivée de l’enfant en salle .
Préparation de la VVP (purgée ++++),tubulure munie d’un robinet à trois voies .
A l’arrivée de l’enfant une vérification ultime permet le contrôle de son identité, son âge, son poids, la durée du jeun.
Technique d’induction
Induction par inhalation
C’est peut être ce moment là, ou l’anesthésie pédiatrique se spécifie par rapport à l’adulte
Technique traditionnelle
Commencer par un mélange, de N2O et d’O2 à 50 %, l’halotane est introduit à 0,25% puis augmenté par palier de 0,25 % toutes les mn ; jusqu’a 2,5 –3% .
Au stade du myosis serré, dès lors la mise en place d’une VVP est possible.
A ce stade la principale cause d’obstruction des VAS est une obstruction de l’oropharynx par le relâchement du muscle génioglosse et donc la chute en arrière de la langue; pour y remédier
- La luxation du maxilaire inférieure en avant
- L’application d’une pression positive.
Au stade de narcose profonde insertion de la canule de Guedel,
le choix de sa taille prévient les incidents,
- trop petite elle aggrave l’obstruction en refoulant la langue en arrière,
- trop grande elle déclenche un laryngospasme,
- sa longueur est apprécié en plaçant la canule contre la joue, son extrémité doit se trouver en contact avec l’angle de la mandibule .
Induction par « single breath »
Avant l’induction le circuit est saturé avec un mélange de N2O /O2 à 70% et d’halotane à5% ;
On demande à l ‘enfant d’effectuer une expiration puis une inspiration profonde après application du masque, dès la perte de conscience l’halotane est ramené à 1.5%
- Intérêt : la rapidité de la narcose = au thiopental
- Inconvénients: absence de coopération de l’enfant, et risques d’une induction à l’halotane à des [ ] élevées.
Le choix de l’halogénés
Sévoflurane meilleur choix.
Tolérance respiratoire ++
Le sévoflurane est plus dépresseur respiratoire que l’halotane, une apnée survient rapidement, elle est mixte :
- centrale
- mécanique ( la chute de la langue).
Tolérance cardiovasculaire
les effets chronotropes, bathmotropes, inotropes (-) de l’halotane ⇒ les hypotensions, les bradycardies, et donc les chutes du débit cardiaque lors des inductions.
l’atropine étant de ce fait systématique !
le Sévoflurane comme tous les halogénés, est un dépresseur myocardique ; moindre qu’avec l’halotane chez l’enfant et le nourrisson
Avec le sévoflurane :
Débit cardiaque maintenu, les PA systémiques sont diminuées, la pression artérielle diminue moins .
Il est moins bathmotrope, chronotrope et dromotrope que l’halotane .
assure une meilleure stabilité hémodynamique durant la phase d’induction.
Avec la technique progressive : augmentation progressive toutes les 30 secondes jusqu'à une concentration de 7 à 8 % pour le sévoflurane et de 5 % pour l’halotane , la vitesse d’induction reste identique(1.6 min contre 1.5min), ainsi que celle de l’intubation(10 min dans les deux cas).
Technique rapide : 7 à 8% d’emblée !
La vitesse d’induction n’est pas différente selon les tranches d’âges : 0.8 min. Une intubation peut être réalisée dans les 4 min qui suivent le début de l’induction .
Induction intraveineuse
Technique
l’abord veineux est indispensable à toute anesthésie pédiatrique
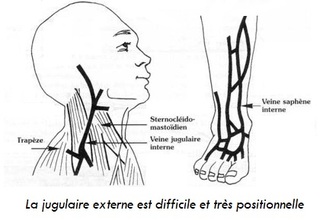
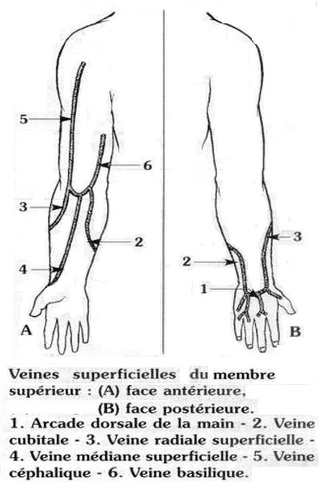
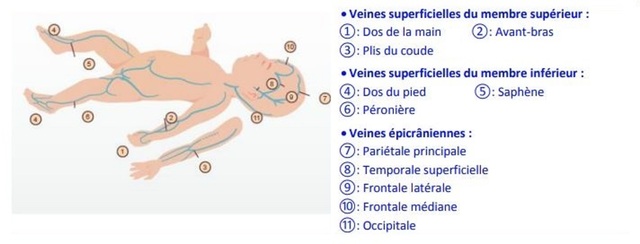
Le site de ponction est en général le dos des mains, le plis des coudes et la tête ( les veines du cuir chevelu sont d’accès faciles chez le n.né).
Le matériel est usuellement des cathéters de 24 G ( jaune ) pour les moins de 12 mois, de 22G (bleu) avant 2 ans , 20 G ensuite ……………. .
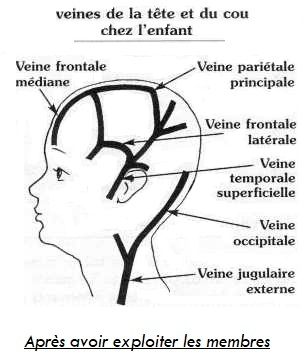
Reconnaître le patient difficile à perfuser
La prise de voie veineuse est reconnue comme difficile chez l’enfant et le nourrisson, chez les patients obèses et les patients de couleur sombre.
La difficulté augmente quand l’enfant a peur de l’aiguille ou a eu de mauvaises expériences, car l’anxiété active le système nerveux sympathique, provoquant ainsi une vasoconstriction locale périphérique. Depuis peu, il existe un score de prédiction de la difficulté de perfusion en pédiatrie DIVA Score (Difficult Intravenous Access Score).
Dès l’obtention d’un score de 4 (min 0, max 10), le taux d’échec est attendu comme étant de 50 % à la 1ère tentative .
Il est remarquable de constater que dans cette étude incluant 615 enfants de 0 à 21 ans, ni la présence d’une peau sombre, ni les impressions subjectives de difficulté à piquer (jugement variable entre les opérateurs), ni la non-utilisation d’alcool ne modifiaient la qualité du score.
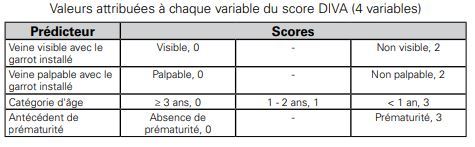
Un score de DIVA de 4 correspond un taux de succès au 1er essai de 50 %.
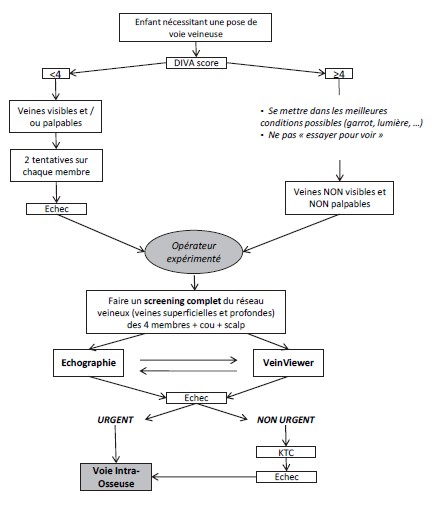
Voie jugulaire externe
Pas toujours aisée chez le petit nourrisson, mais peut être une bonne alternative sur un échec de VVP. Si la veine est plate, la comprimer au niveau du creux sus claviculaire pour la faire gonfler.
Ponction intra osseuse
Indication en urgence
- ACR, mort subite, hypovolémie (polytraumatisme, déshydratation...),
- Si échec après 2 ou 3 tentatives d’accès veineux périphériques : chocs septique ou cardiogénique, brûlure étendue, noyade …
3 sites d’insertion
- Tibia proximal : face antéro-interne, 1 à 2 cm sous la tubérosité tibiale
- Tibia distal : juste au-dessus de la malléole interne
- Fémoral inf. (Jamshidi® ou EZ-IO® )
Humérus proximal : au niveau de la tête humérale (uniquement avec foreuse EZ-IO® ). A éviter chez l’enfant < 10 ans
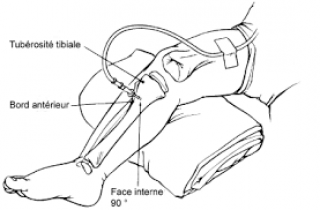
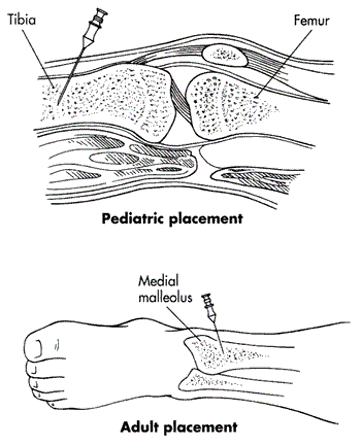
Technique
- Asepsie, décubitus dorsal, jambe en légère rotation externe, posée sur un billot ou sur sa main
- Anesthésie locale possible selon les circonstances ou sous entonox
- Aiguille de Jamshidi® (biseau dirigé vers le bas), insérée perpendiculairement à l’os et légèrement inclinée vers le bas pour ne pas embrocher le cartilage de conjugaison.
- Quand l’aiguille atteint l’os, exercer une pression ferme, en imprimant des mouvements de rotation jusqu’à ressentir son insertion dans la moelle (attention : plus le nourrisson est petit, moins on perçoit cette sensation)
- Aiguille EZIO® avec des aiguilles roses puis bleu pour < 35 kg et jaune pour les adultes et grands enfants
Vérification
- L’aiguille doit tenir tout seule +++ Aspiration de moelle osseuse à la seringue
- Injection facile de NaCl 9 ‰ à la seringue, sans infiltration sous-cutanée
Perfusion
- Utiliser un PSE ou une poche à pression pour avoir un débit suffisant Tous les produits de remplissage et / ou médicaments sont administrables par cette voie
Complications
Echec par coudure de l’aiguille, fracture du tibia, extravasation sous-cutanée (syndrome des loges), occlusion du cathéter, infection (ablation systématique après 12 - 24 h)
Agents intraveineux
L’étomidate (HYPOTOMIDATE®)
Sa demi-vie d’élimination plus courte que chez l’adulte,
Contre-indiqué en dessous de 2 ans : il subit une hydrolyse par les estérases hépatiques produisant de l’acide carboxylique inactif éliminé par voie urinaire .
Malgré des phénomènes d’excitation à l’induction, ce produit est intéressant par sa bonne tolérance hémodynamique pour les terrains fragilisés (hypovolémies cardiopathies ).
Il n’est pas conseillé de l’utiliser en continu car il est à l’origine d’une inhibition cortico-surrénalienne qui persiste plusieurs heures après une administration prolongée.
| Age |
Dose |
|
7-13 ans
|
0.3-0.4 mg/Kg
|
| Adulte |
0.2-0.3 mg/Kg
|
Le thiopental (NESDONAL®)
Plus grande sensibilité du nouveau né au thiopental(captation cérébrale d’autant plus rapide que le débit sanguin cérébral est plus élevé, hypoalbuminémie et augmentation de la fraction libre). Le métabolisme se faisant par oxydation hépatique .
Il n’y a pas d’effets secondaires spécifiques pédiatriques
| Age |
Doses (mg/kg)
|
Dilution(%)
|
|
Nouveau né
|
3-5 |
1% |
| 1-6 mois |
10 |
2.5% |
| 6-12 mois |
8-10 |
| > 12 mois |
6-8 |
| adulte |
3-4 |
C’est l’agent de référence (dans les études pharmacologiques), administré en solution de 2.5% (25 mg/ml), la dose dépend de l’âge ( plus élevé chez l’enfant petit), la dose préconisée est de 10 mg/ kg jusqu'à 6 mois , de 8 à10 mg/kg entre 6 et 12 mois et de 6 mg/kg au delà de 1 an .
Le propofol (DIPRIVAN®):
La clairance et la demi-vie sont sensiblement identique à l’adulte le VD étant le double de l’adulte, d’ou augmentation des doses et des concentrations sériques pour maintenir une anesthésie efficace (le double de l’adulte),
le métabolisme est hépatique ( réactions de conjugaison).
|
Age
|
Induction( mg/Kg)
|
<30 min(mg/Kg/h)
|
>30 min(mg/Kg/h)
|
|
> 1 mois
|
4-6
|
|
|
|
< 3 ans
|
4-6
|
|
|
|
> 3 ans
|
3.5-5
|
15-18
|
12-15
|
|
adulte
|
2.5
|
10-15
|
10
|
|
Doses préconisées sont de 3.5 à 5 mg/kg, comparativement au thiopental le rapport de doses d’induction de propofol est de1/2.5
L’augmentation des doses s’explique par une augmentation du volume de distribution du compartiment central.
Deux incidents grève l’utilisation du Propofol : la douleur à l’injection (adjonction de 1ml de xylocaine à 1% pour 20 ml de propofol). et les phénomènes d’excitation .
Les modifications hémodynamiques après injection de 2.5 mg/kg de propofol, et de 5 mg/Kg de thiopental sont superposables : la baisse de la pression artérielle est secondaire à la chutes des résistances vasculaires systémiques .
La kétamine (KETALAR®)
Métabolisme hépatique .
L’hypersécretion bronchique est responsable, chez le nourrisson de spasmes laryngés ou d’un encombrements respiratoires imposant la prescription d’atropine .
Les phénomènes hallucinatoires associés justifie la prémédication par les benzodiazépines .
|
Age
|
Voie IM (mg/kg)
|
Voie IR
|
Voie IV
|
Voie IV cont.
|
|
< 3 mois
|
10
|
8-10
|
1-2
|
2-3
|
|
3-12 mois
|
|
4 ans
|
2-3
|
|
4-9 ans
|
|
adulte
|
Intubation
Justification de l’intubation
En dehors de toute nécessité chirurgicale, l’intubation endotrachéale peut se justifier par les particularités anatomiques et physiologiques .
5 Particularités anatomiques (en laryngoscopie directe)
- le larynx de l’enfant est plus antérieur , plus haut situé (C3-C4)
- la langue est plus large, gène la vision laryngoscopique directe, la distance plus courte entre la base de la langue et le voile du palais explique une obstruction plus facile par la chute en arrière de la langue .
- l’épiglotte en oméga et difficile à contrôler avec la lame.
- le plan des cordes vocales est oblique en bas et en dedans , explique que l’extrémité de la lame butte souvent sur leur commissure antérieure.
- la présence de la sténose sous-glottique.
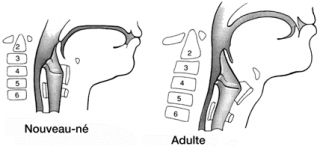
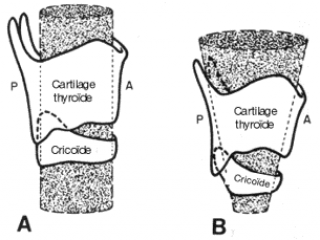
Particularités physiologiques
La justification physiologique respiratoire est une seconde raison pour l’intubation :
le rapport ventilation alvéolaire / capacité résiduelle fonctionnelle est plus important que chez l’adulte .
Les réserves en oxygène sont basses face à une consommation élevée (en flux tendu !)
On comprend dès lors la rapidité des épisodes hypoxiques
Règle : intubation chez l’enfant de < de 1 an si intervention >30 min
Matériel
Laryngoscope :
Les lames de Miller (droites ) ,pour les enfants de 0 à 6 mois ,ensuite les lames sont courbes et adaptées à l’âge ( bon sens !).
Les sondes d’intubation (sans ballonnet) :
|
|
Diamètre int.
|
Longueur(cm)
|
|
Orotrachéale
|
nasotrachéale
|
|
Nouveau né
|
2.5-3
|
|
7+1/kg
|
|
1 – 3mois
|
3-3.5
|
10 –11
|
11- 12
|
|
6 mois
|
4
|
12
|
13
|
|
1 an
|
4 –4.5
|
13
|
14
|
Le tableau est seulement indicatif
Taille des sondes, numérotée en fonction de leur diamètre externe(CH=charrière ou F=french); le choix dépend de l’âge de l’enfant .
Des la première année de vie la formule suivante est appliquée :
Taille de la sonde (charrière) = 20 + âge (en années)
Pour toute intubation, il faut prévoir 3 sondes :une sonde supposée par rapport à l’âge ,une de diamètre inférieur, et une de diamètre supérieur.
Pour que la sonde trachéale soit en bonne position, il faut que son extrémité se situe au milieu de la trachée chez le nouveau né :la vérification de la bonne position de la sonde s’effectue en premier lieu par l’auscultation, si l’enfant doit rester intubé longtemps un contrôle radio est indispensable .
longueur d’intro./arcade dent. = 10cm+0.5cm par année d’âge
En fait les règles, les formules sont nombreuses, ce qui nous doit nous rendre encore plus vigilant qu’au choix de la sonde.
La sonde idéale est celle qui permet une ventilation adéquate en permettant une fuite pour des pressions de 20 cm d’eau, il est donc indispensable d’avoir à proximité des sondes de diamètre supérieur et inférieur .
Les sondes sont en PVC à la chaleur elle ont tendance à se ramollir.
Longueur d’intro./l’aile du nez = 7 +1 cm/Kg de poids
sonde avec ou sans ballonnet : la polémique?!
Les risques liés à l’utilisation de sondes d’intubation avec ballonnet
Les raisons invoquées pour justifier l’utilisation de sondes sans ballonnet chez l’enfant de moins de 8 ans sont aux nombres de trois :
- l’addition d’un ballonnet réduit le diamètre utile de la sonde d’intubation, et augmente le travail ventilatoire en ventilation spontanée ;
- les ballonnet risquent de léser la muqueuse trachéale, et donc augmente le risque de complications respiratoire à l’extubation ;
- les ballonnets ne sont pas nécessaires chez le jeune enfant car le rétrécissement cricoidien permet d’assurer une étanchéité des voies aériennes supérieures si la sonde est de taille adéquate
Les risques liés à l’utilisation de sondes d’intubation avec ballonnet
Ces arguments doivent être revus en fonctions des données de la pratique quotidienne et de la littérature depuis une décennie :
Dans la littératures , il existe 2 études , la dernière en date ,est celle de Khine, portant sur 251 enfant de mois de 8 ans intubés avec une sonde à ballonnet et 237 avec une sonde sans ballonnet , la fréquence des complications respiratoires a été dans les deux groupe identique (1%), ,par contre ,il a été nécessaire de reintuber 54 patient dans le groupe sans ballonnet (23%) en raison du calibre mal adapte et seulement 3 patient dans le groupe avec ballonnet (1.2%).
L’autre justification est l’augmentation du travail ventilatoire en ventilation spontanée par la diminution du diamètre interne (utile) généré par le ballonnet , en fait c’est vrai si on suit la loi de Poiseuille (R= Cst X l X 1/r4), mais c’est une absurdité sur le plan physiologique (pas de ventilation spontanée avec une intubation !(voir physio)donc cet argument ne tient pas .
Avantages de l’utilisation de la sonde d’intubation à ballonnet :
Si les inconvénients sont difficiles à identifier les avantages sont plus faciles à présenter :
- La mise en place d’une sonde à ballonnet permet d’éviter les réintubations pour les pour les fuites et d’utiliser un débit faible de gaz frais et donc de réduire la pollution des blocs opératoire et le coûts des agents anesthésiques.
- L’absence de réintubation , limite les tentatives d’intubation et le risque potentiel de traumatismes .
- La présence du ballonnet semble limiter les inhalations dans les périodes d’urgences (ventre plein ) .
Bonnes pratique clinique de la sonde à ballonnet :
En pratique quand on utilise des sonde à ballonnet, on choisit une sonde d’une taille inférieure à celle d’une sonde sans ballonnet (les tailles de sondes indiquent le diamètre interne en mm).
Chez l’enfant de plus de 2 ans Khine a choisit la formule ;
- Sonde à ballonnet (Di en mm )= (âge en années /4)+3
- Sonde sans ballonnet (DI en mm) = (âge en années /4)+4
En dessous de l’âge de 2 ans, on propose une sonde de 3 jusqu'à 5 kg et de 3.5 au delà de 5 Kg .
Le franchissement du cartilage cricoïde doit se faire sans frottement et l’extrémité supérieure du ballonnet doit être placée en dessous des cordes vocales.
Le monitorage comporte systématiquement
- la fraction télé-expiratoire en CO2 ;
- le volume inspiré (Vi)et le volume expiré (Ve), la différence entre Vi et Ve permet d’apprécier la fuite, le gonflage du ballonnet doit permettre de limiter ces fuites sans toutefois les éteindre(sauf cas du ventre plein).
Le monitorage de la pression du ballonnet est important quand on utilise le N2O, si on utilise de l’air, son volume va augmenter dans le temps, et donc la pression exercée sur la muqueuse trachéale , car le protoxyde d’azote diffuse plus facilement, si le ballonnet est gonflé avec un mélange air protoxyde la pression reste inchangée au cours du temps , en pratique il faut dégonfler le ballon et le regonfler avec le mélange prélevé au niveau du filtre .
« Réflexion »
La règle pas de ballonnet en pédiatrie, ne semble plus valable , le choix doit résulter d’un rapport bénéfices /risque , les effets délétères potentiels d’une pression excessive sur la muqueuse sont à mettre en balance avec les avantages des sondes .
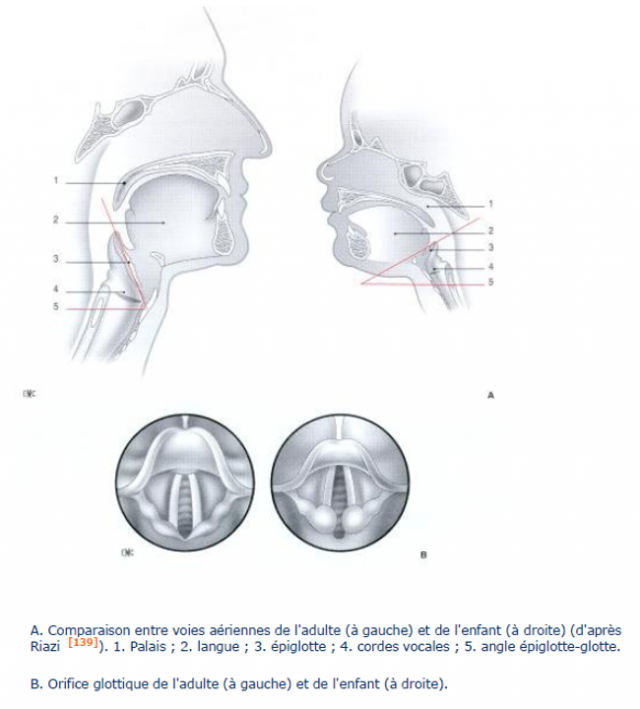
Comment réaliser une intubation
La dénitrogénation
C’est une règle de sécurité :la faible capacité résiduelle fonctionnelle respiratoire (réserve en oxygène) ,face à une consommation d’oxygène élevée explique la rapidité de la survenue des épisodes hypoxiques.
Si la dénitrogénation n’est plus remise en cause, sa durée reste à déterminer . ; après une oxygénation de 1 min, le temps de survenue de la désaturation à 95 % est de 77 +/-20 secondes ,après 3 min le temps est de 120+/-34 secondes .
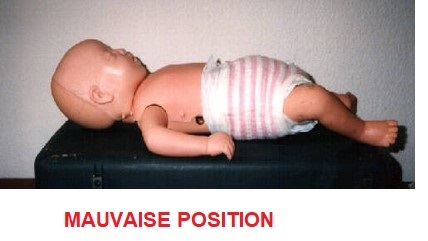
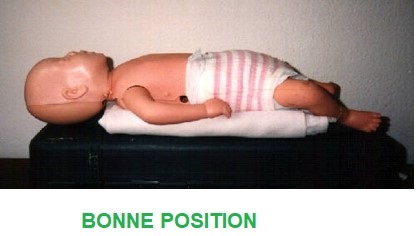
Placer la tête de l’enfant
C’est la clé d’une intubation réussie, cette bonne exposition demande une position neutre de la tête avec une légère extension pour aligner les trois axes, laryngés, pharyngé, et trachéal, pas de nécessité de surélever la tête, car l ‘axe fronto occipital et supérieur à celui de l’axe interro postérieur du thorax.
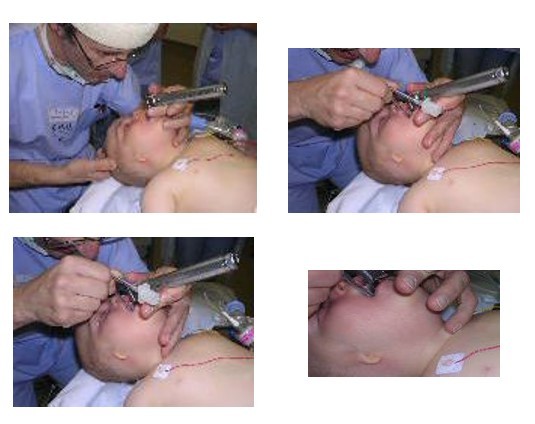

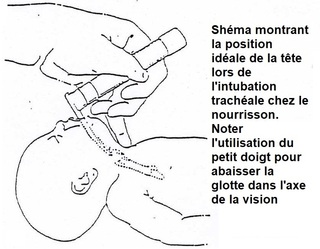
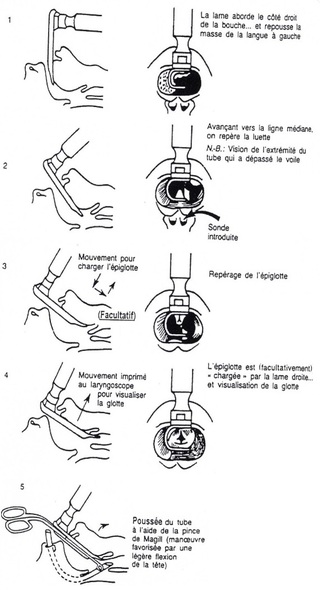
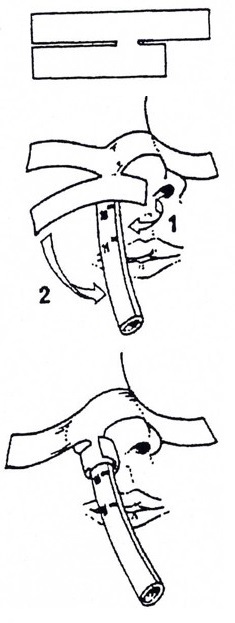
Curares ou pas ?
Les arguments pour la curarisation sont : la qualité des conditions d’intubation .
Les arguments contres sont ceux des effets secondaires des curares ……
Quels curares ?
La succinylcholine (célocurine®) :
Sa posologie est augmentée chez le nourrisson(2mg/kg)malgré la baisse du taux des pseudocholinestérases plasmatiques qui l’hydrolysent, (augmentation du volume de distribution).
L’administration intramusculaire à la dose de 4mg/kg est possible en l’absence de voie veineuse ( délai long de 4 minutes et action prolongée 20 minutes).
On n’observe pas chez l’enfant de moins 4 ans des fasciculations par contre les bradycardies sont plus fréquentes (hypertonie vaguale ).
Les agents non dépolarisants
Les particularités pharmacocinétiques en fonction de l’âge sont comparable pour différents agents.
L’augmentation du Vd chez les plus jeunes contrebalance la plus grande sensibilité aux myorelaxants du nouveau né et du nourrisson ; la clairance est peu influencée par l’âge .
En règle générale, les doses sont plus faibles dans la première année et la durée d’action est plus courte chez l’enfant de 4 à 6 ans .
Tous les curares sont potentialisés par les halogénés; Il existe une variabilité interindividuelle importante qui légitime le monitorage de la curarisation.
Le mivacurium (MIVACRON®): est une benzylisoquinoline dégradée par les cholinestérases plasmatiques dont le déficit provoque un bloc prolongé(1/25000).
Le vécuronuim (NORCURON®) : est un stéroide faiblement métabolisé par le foie et éliminé par la bile d’ou son accumulation chez le nné (durée d’action double de celle de l’enfant de plus de 8 ans :60 min contre 30 minutes .
L’atracrium (TRACRIUM®) : est une benzylisoquinoline dégradée par la réaction d’hoffman et des estérases non spécifiques ce qui explique l’absence d’accumulation. l’histaminolibération existe mais plus faible que chez l'adulte
|
Enf.> 1an
|
Poso./intub.
|
Délai
|
durée
|
Poso /reinj.
|
|
Mivacron®
|
0.2
|
< 2 min
|
< 20 min
|
0.1/6-9 min
|
|
Norcuron®
|
0.15
|
=2 min
|
30 min
|
0.02-0.03
|
|
Tracrium®
|
0.6
|
1.5 – 2 min
|
25-35 min
|
0.3-0.6
|
|
Esméron®
|
0.6
|
1-1.5 min
|
= 40 min
|
0.15
|
|
Nimbex®
|
0.1
|
2.5-4 min
|
45-60 min
|
0.02/10 min
|
|
Pavulon®
|
0.07-0.1
|
2.5-4 min
|
90 min
|
0.015
|
La Célocurine® reste encore le curare référence dans le cadre de l’estomac plein.
Les alternatives à l’utilisation de la Célocurine :
Les curares non-dépolarisants : En utilisant un autre curare dans les conditions de l’urgence on s’expose à en payer le prix ! ; Le rocuronium à la posologie de 1.5 mg/Kg offre des conditions moindres que la Célo, à des doses plus élevées , les conditions sont superposables mais les délais sont 2 à 3 fois plus longs .
Elle reste le seul curare qui permet une décurarisation avant la survenue d’une hypoxie devant une intubation impossible non prévue (valable pour le grand enfant).
L’estomac plein :
Il s’agit d’une situation à risque, elle est superposable à l’adulte :
Espérer un délai de 6 heures pour les plus grands,
Les anti H2 (Cimétidine ) 2 à 3 heures avant élèvent le pH sans éviter l’inhalation.
La vidange gastrique est indispensable surtout chez le nourrisson dont l’alimentation est liquide
La séquence d’ induction doit être rapide
Préoxygénation de 3 min
Thiopental 4 - 6mg/kg
Célocurine 2 mg/kg
Maneuvre de sellick
En pratique la Celocurine® le thiopentothal peut être remplacé par le Diprivan®.
Particularités « pédiatrique » de l’indication de la curarisation
- La curarisation ne rend pas plus facile l’intubation trachéale chez l’enfant .
- Aucune étude ne permet de dire que l’incidence des complications soient différentes avec ou sans curare .
- Les effets de la succinylcholine sont plus importants chez l’enfant et d’autant que l’enfant est plus petit : arrêt cardio-circulatoire , spasme des masseters, hyperthermie maligne (en association avec l’halothane ).
- La curarisation :
- En chirurgie programmée :
- Chez l’enfant sans difficultés prévisibles d’intubation lorsque la curarisation n’est pas utile en per op : pas de curare
- Inversement préférer le curares d’action intermédiaire
- Chez l’enfant ,avec intubation potentiellement difficile : l’intubation se fera en ventilation spontanée par sevoflurane ou propofol.
- ventre plein → Celocurine® !
Les anticholinestérasiques :
Uniquement représentés par la néostigmine (PROSTIGMINE®) dont la demi-vie est plus courte chez le nourrisson et l’enfant que chez l’adulte ; les doses sont moindres que chez l’adulte (30µg/Kg au lieu de 40-50µg/kg).du fait des différence locales au niveau de la jonction neuro-musculaire .
L’atropine doit y être associée (dans la même seringue ) à la dose de 20µg/Kg.
Les traumatismes :
Dentaires des dents de lait avant l’âge de 7 ans
laryngé résultat d’un diamètre inadapté de la sonde d’intubation il est prévenu par le test de fuite
Le laryngospasme
Conduite à tenir devant un laryngospasme peranesthésique chez l’enfant
1°- Incidence et facteur de risques :
Dans une étude de 2000, l’incident le plus fréquemment rencontré, est le laryngospasme (25%), cet incident lié à l’anesthésie, peut par son caractère soudain et imprévisible, peut avoir des répercussions dramatiques si une prise en charge rapide et efficace n’est pas instaurée.
La population la plus exposée est la tranche d’âge des 1 à 3 mois , avec cependant un « écart type » large de 0 à 9 ans.
Facteurs de risques
- Le tabagisme passif ,
- une infection des voies aériennes supérieures ,
- l’inexpérience ,
- la chirurgie ORL.
2°- Physiopathologie :
Interruption involontaire et prolongée de la perméabilité laryngée intervenant le plus souvent pendant la phase expiratoire .
Intervention des structures glottiques et supraglottiques :
- Les cordes vocales + les replis aryténoïdes ,
- Sous la dépendance de ⇒ musculature intrinsèque et extrinsèque du larynx .
La musculature intrinsèque est innervée par le nerf récurent et le nerf laryngé supérieur (branche de la X ème paire crânienne),
Les muscles adducteurs des cordes vocales sont sous la dépendance du nerf récurent ;
L’unique muscle intrinsèque abducteur des cordes vocales (muscle cricothyroïdien)dépendant du nerf laryngé externe (sensitivomoteur )provenant lui même du nerf laryngé supérieur, principal nerf sensitif du larynx
Ainsi toute stimulation sensitive laryngée est susceptible par l’intermédiaire du nerf laryngé supérieur de déclencher une contraction réflexe à l'origine du laryngospasme .
Parmi les muscle extrinsèque le muscle thyroïdien joue un rôle important dans la genèse du laryngospasme .
En effet si son rôle principal est d ‘assurer la stabilité longitudinale des structures laryngées , sa contraction lors d’un laryngospasme provoque un tassement des structures supraglottiques contribuant à l’interruption de la filière laryngée supraglottique .
Cela permet de mieux comprendre pourquoi l’étirement des muscles thyrohyoidïen induit par la luxation antérieure du maxillaire inférieur constitue l’une des première mesure susceptible de lever un laryngosaspme .
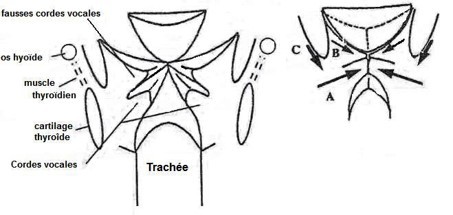
-
Même en simplifiant à l’extrême la physiopathologie , le modèle animal apporte quelque donnée : l’hypoxie , l’hypercapnie et des pression positives intrathoraciques augmentent le seuil de déclenchement et inhibe ainsi sa survenue ou sa pérennisation .
A l’inverse son seuil de déclenchement est abaissé par une hypocapnie, ou une pression négative intrathoracique .
L’hyperoxie ne joue aucun rôle déclenchant ou inhibant .
-
3°- conduite à tenir :
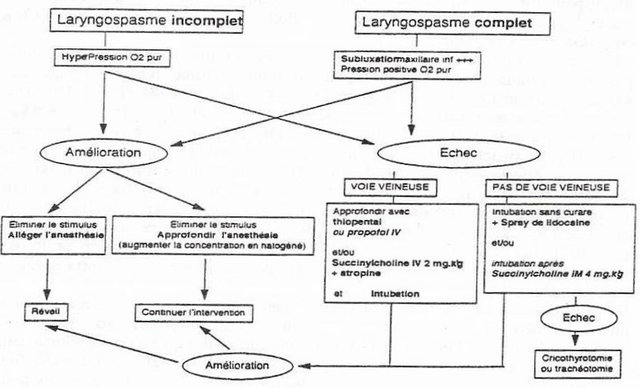
3°- conduite à tenir :
- En cas de laryngospasme peranesthésique incomplet (filière laryngée encore perméable ),
- L’arrêt de toute stimulation ,
- L’application d’une pression positive en oxygène pur permet en général de passer le cap ;
- Une augmentation de la concentration des halogénés permet de compléter la levée du laryngospasme .
- En cas d’echec de l’insufflation d’oxygène (désaturation), la prise en charge suit l’algorithme du laryngospasme complet.
- En cas de laryngospasme complet :
- Subluxation du maxillaire inférieur +++ indispensable, (car en étirant le muscle thyro-hyoidien on s’oppose à son action constrictive sur les structures supraglottique d’ou perméabilité des VAS).
N.B: une pression positive forte (valve de ruben) sans luxation provoque une surpression dans la fosse pyriforme, et majore la compression des structures supraglottiques et renforce l’étancheité du laryngospasme .
A ce niveau, la conduite à tenir dépend avant tout de la présence ou non d’une voie veineuse fiable ou pas .
- Si une voie veineuse est présente:
- approfondissement de l ‘anesthésie (hypnotique et curares).
- Sans voie veineuse,
- La célocurine en IM ou intraosseuse: pas assez de recul
- Les autres curares (non dépolarisants)par voie IM, sont formellement contre-indiqués dans cette situation d’urgence , leur efficacité n’apparaît que 15 minutes après ! ! .
- Intubation sans curares , car forte probabilité d’une ouverture glottique consécutive à l’hypoxie, et à l’hypercapnie inévitable ! .
- Dernier recours La trachéotomie car très grande morbidité de la technique .
4°- La prévention
-
Le laryngospasme survient dans 88% au cours de l’induction , 23% lors du réveil, et notamment lors de l’extubation (12%).
Si pour certain la qualité de l’anesthésie et l’expérience de l’opérateur (médecin /iade), l’utilisation de nouveaux agents anesthésiques pourrait modifier ces chiffres mais rien de probant.
Parmi les agents intraveineux, seul le propofol semble supérieur au pentho, (pas de consensus).
L’utilisation d’anesthésie locale lors d’une intubation a permis de diminuer l’incidence des laryngospasme lors de l’extubation