- Accueil
- Modules 1ére année
- 5. ANESTHÉSIE & SOINS POST-OPÉRATOIRES SELON LE TERRAIN & LE TYPE DE CHIR, Part 1(Vh: 92 h, Coef :3)
- 5.1.7. Anesthésie du patient présentant une pathologie cardiaque et vasculaire ;
5.1.7. Anesthésie du patient présentant une pathologie cardiaque et vasculaire ;
F. Le Corre, J. Marty EMC - Anesthésie-Réanimation Volume 13 > n◦1 > janvier 2016-Arrangement MS.BENELMIR
Introduction
Vieillissement de la population + Sédentarité + Prise en charge médicale insuffisante
=
Patients avec des pathologies cardiaques de gravité variable, en particulier des insuffisances cardiaques non diagnostiquées
Prévalence
2 à 5 % dans la population générale
10 à 15 % au-delà de 80 ans
La survie à cinq ans est supérieure à 30 %.
Morbimortalité péri opératoire
IC (9%=) > coronaropathies (2,5 %)
(prise en charge préopératoire moins formalisée??)
l’Office national des statistiques (ONS), au troisième trimestre 2018, placent les cardiomyopathies en 1ére position /au nombre global des décès dus aux maladies, avec un taux de 41% (40% en 2017)*.
*Pr Naïma Hammoudi, présidente de la Société algérienne de cardiologie (SAC), 21e Congrès maghrébin de cardiologie 11-2018
Définition
Incapacité du cœur à fournir un apport sanguin suffisant pour répondre aux besoins métaboliques de l'organisme, caractérisée par une diminution de la capacité cardiaque à l'effort.
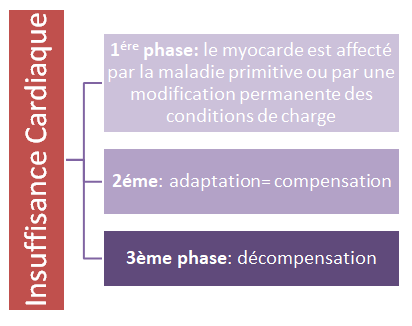
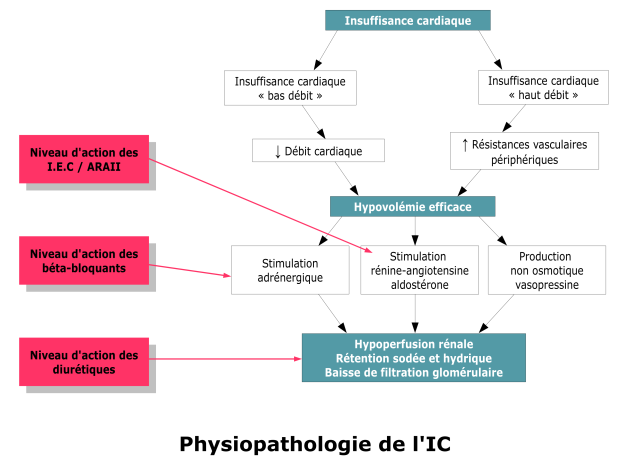
Physiopathologie
Le premier symptôme habituel de l'insuffisance cardiaque est l'essoufflement à l'effort ; avec l'évolution de la maladie, cet essoufflement devient permanent.
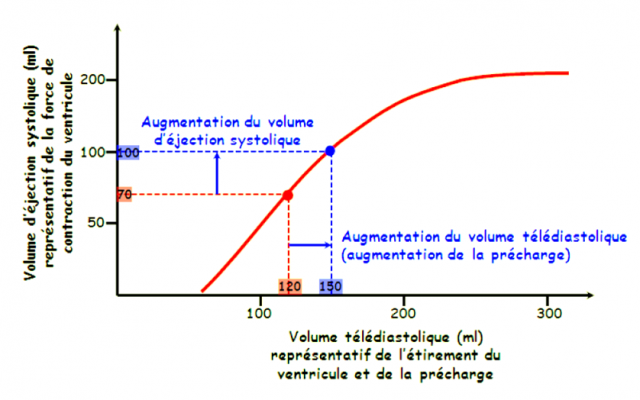
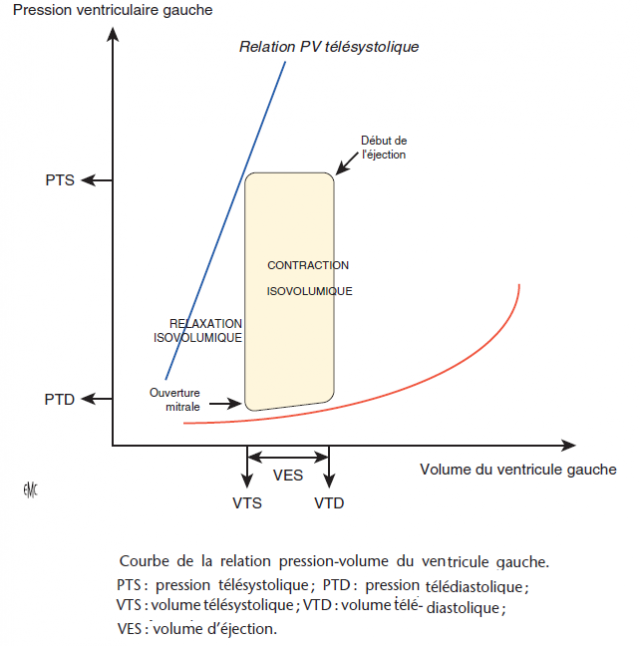
- La baisse de la performance ventriculaire met en jeu la réserve de la précharge (loi de Franck-Starling).
- L’élévation du VTD et de la P° télédiastolique permet de maintenir, au moins dans un premier temps, le VES .
Loi de Frank-Starling
Selon la Loi de Frank-Starling (ou relation deFrank-Starling), plus le volume télédiastolique d'un ventricule augmente, plus l'énergie produite par ce dernier pour éjecter le sang sera grande. Elle prédit l'augmentation progressive de la force de contraction au fur et à mesure que le remplissage ventriculaire s'opère.
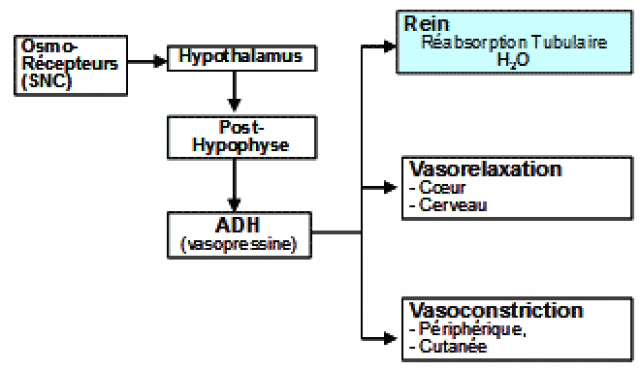
- Ce phénomène est provoqué par une veinoconstriction (activation du système Σ ) et par une rétention hydrosodée consécutive à la stimulation du SRAA.
- L’élévation des pressions en amont du ventricule malade entraîne des signes congestifs. La prescription d’un régime peu salé et l’utilisation de diurétiques ont pour but de réduire l’intensité de ces phénomènes.
En réaction aux modifications des conditions de charge
↓
hypertrophie des myocytes + modification structurelle de la Ȼ
↓
↓tension pariétale
↓la charge et ↓ dépenses énergétiques myocardiques
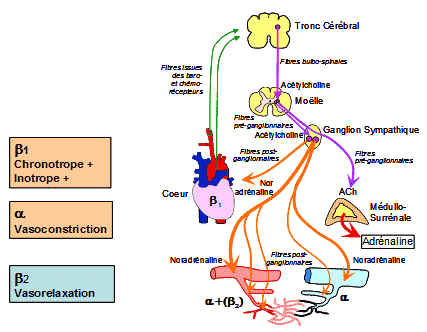
Stimulation du Σ
↓
Tachycardie + vasoconstriction artérielle
↓
↑dépenses énergétiques + Altération de la pompe du Cœur gauche
=
↑ post charge
| Mécanisme | Bénéfice | Inconvénient |
|---|---|---|
|
Rétention hydrosodée |
Augmente la précharge |
Signes de congestion |
| Vasoconstriction |
Maintien de la pression artérielle |
Majore la dysfonction ventriculaire |
|
Stimulation sympathique |
Augmente la FC et l’inotropisme |
Majore la dysfonction ventriculaire, la dépense énergétique |
| Hypertrophie |
Réduit la tension pariétale |
Augmente la dépense énergétique, altère la fonction diastolique |
L’augmentation chronique de l’activité Σ
=
phénomène de désensibilisation
=
↓de la densité des récepteurs bêta-1 du myocarde
+
hyporéactivité aux agonistes bêta-1.
•L'insuffisance cardiaque débute habituellement par une altération de la fonction du ventricule gauche. Son évolution se fait vers une stase pulmonaire, hypertension artérielle pulmonaire, puis retentissement sur le cœur droit avec insuffisance cardiaque droite.
L'insuffisance cardiaque congestive
Correspond à l'association des insuffisances ventriculaire gauche et cardiaque droite avec HTAP et retentissement sur le retour veineux (œdèmes).
Le syndrome de bas débit cardiaque
C’Est une variété de choc cardiogénique dans laquelle la baisse du débit cardiaque (FEVG) est consécutive à une inefficacité des contractions du myocarde suivie d'une vasoconstriction.
Les autres symptômes accompagnateurs sont une HTA modérée et une augmentation de la pression veineuse.
Dans certaines formes le débit cardiaque est normal voire élevé, le déficit en transport d'O2 par ↓ d‘Hb nécessite une ↑ du débit cardiaque pour assurer une bonne oxygénation périphérique.
La FC est ↑, les extrémités sont chaudes, il y a des signes de congestion pulmonaire avec parfois ↓ TA .
Dans :
- Anémies
- Déficits en thiamine (béri-béri),
- Fistules artério-veineuses, dans les
- Formes évoluées de la maladie de paget,
- Les hyperthyroïdies...
Etiologie
Maladies du myocarde
Primitive
- Cardiomyopathie idiopathique
Secondaires
- Insuffisance coronaire
- Collagénose (lupus, périartérite noueuse, dermatomyosite, sclérodermie, etc.)
- Maladies endocriniennes (hypothyroïdie, hyperthyroïdie, acromégalie,
- Phéochromocytome)
- Maladies génétiques
- Médicaments (chimiothérapie)
- Maladies infectieuses
- Maladies neuromusculaires
- Rhumatisme articulaire
- Autres maladies systémiques (amylose, etc.)
Anomalies mécaniques
Surcharge en pression
- Hypertension artérielle
- Rétrécissement aortique
Surcharge en volume
- Insuffisances aortique et mitrale
- Fistule artérioveineuse
- Communication interauriculaire ou interventriculaire
- Béribéri.
Évaluation préopératoire
L’objectif de L’évaluation préopératoire est la diminution du risque périopératoire.
En dehors de l’urgence vitale, cette évaluation peut nécessiter de 1 à 6 semaines en préopératoire (American College of Cardiology/American Heart Association [ACC/AHA]).
Évaluation clinique
Son but est de détecter ou diagnostiquer la cardiopathie
- L’interrogatoire →dyspnée, orthopnée, la capacité d’effort
- les antécédents→ œdème pulmonaire aigu, troubles du rythme, etc.
- La classification NYHA voit sa limitation dans la difficulté liée à la capacité d’effort chez des personnes ayant perdu leur autonomie en raison de l’âge ou de limitation articulaire par exemple
|
Classification de la New York Heart Association. |
|
|---|---|
| Classe I |
Aucune gêne fonctionnelle, y compris à l’effort |
| Classe II |
Limitation fonctionnelle pour les efforts importants, pas de gêne au repos |
| Classe III |
Limitation fonctionnelle pour des efforts légers, entravant l’activité ordinaire |
| Classe IV |
Limitation permanente au repos, majorée au moindre effort |
- Le score clinique de Lee est un bon indicateur du risque périopératoire
| Pathologie | Point |
|---|---|
|
Coronaropathie |
1 |
|
Insuffisance cardiaque |
1 |
|
Diabète insulinodépendant |
1 |
|
Insuffisance rénale chronique (créatinine préopératoire > 177 mol/l) |
1 |
|
Accident vasculaire cérébral |
1 |
|
Chirurgie à risque élevé |
1 |
| Chirurgie à risque élevé : chirurgie intrathoracique ; chirurgie intrapéritonéale ; chirurgie vasculaire supra-inguinale. Probabilité de survenue d’une complication cardiaque postopératoire : aucun critère, 0,4 % ; un critère, 0,9 % ; deux critères, 7 % ; plus de deux critères, 11 %. | |
Explorations complémentaires
Son but est d’évaluer la sévérité
- L’échographie-Doppler +++. permet l’évaluation de la fonction systolique ventriculaire gauche
- L’échographie a la recherche des troubles de la cinétique segmentaire, une hypertrophie pariétale et surtout une dysfonction diastolique du ventricule gauche
- La RX pulmonaire a la recherche d’un index cardiothoracique supérieur à 0,5, évocateur d’une cardiopathie évolutive, la redistribution vasculaire vers les sommets, un œdème interstitiel (lignes de Kerley) ou alvéolaire (péribronchique).
- L’ ECG recherche un trouble du rythme ou de la conduction ; il doit figurer dans le dossier pour permettre une comparaison postopératoire.
- Les examens biologiques
Optimisation du traitement
- Elle implique la correction des facteurs aggravants, tels que les troubles de l’équilibre hydroélectrolytiques, l’anémie, la volémie, les troubles du rythme, etc.
- Avis spécialisé cardiologique
- Stratégie possible si respect des délais.
Détermination de la prise en charge
- L’évaluation préopératoire permet de déterminer, en particulier, le monitorage qui sera utilisé en peropératoire
Si l’insuffisance cardiaque est compensée
sous traitement optimal, le monitorage dépend du geste envisagé, en particulier s’il implique des variations hémodynamiques importantes (clampage aortique, clampage du pédicule hépatique, chirurgie thoracique, utilisation de ciment en chirurgie orthopédique, etc.).
Si insuffisance cardiaque décompensée,
- surveillance de la dérivation DII,
- monitorage de la température,
- surveillance continue de la diurèse,
- monitorage continu de la fraction expirée en CO2,
- monitorage invasif de la pression artérielle ;
- cathétérisme de l’artère pulmonaire avec éventuellement monitorage continu de la saturation du sang veineux en O2
- cathétérisme de l’artère pulmonaire avec éventuellement monitorage continu de la saturation du sang veineux en O2
- mesure du débit cardiaque non invasif :
- ETO
- CO2 expiré, (en cours d'évaluation)
- l’étude de la pulsatilité artérielle, //
- le Doppler trans-oesophagien, //
- la bio-impédance thoracique //
- monitorage de la température.
Prémédication et traitements préopératoires
L’agent sédatif utilisé pour la prémédication doit à la fois être suffisamment sédatif pour limiter le retentissement de l’induction de l’anesthésie et ne pas comporter d’effet hémodynamique significatif.
IEC, ARA II
- Les IEC et les antagonistes des récepteurs à l’angiotensine II (ARA II) risque majoré d’hypotension artérielle lors de l’induction de l’anesthésie, lors d’une hypovolémie ou d’une hémorragie, avec une absence d’accélération réflexe de la FC.
- Maintien jusqu’au jour de l’intervention chez le sujet insuffisant cardiaque,(même si l’hypotension à l’induction est plus fréquente).
- S’ils doivent être interrompus, une reprise la plus précoce possible doit être prévue.
Bêtabloqueur
- Ne pas stoppé en raison du risque d’effet rebond.
- Un patient déjà traité → continuer le traitement ;
- Si introduction du traitement → 24 heures avant (idéalement 2 à 7 j, voire 30 j pour certains, pour obtenir l’équilibre)
- Ne pas l’introduire le jour de l’intervention → majoration des manifestations hémodynamiques lors de l’anesthésie,
Diurétiques
- Interrompre la veille.
- Corrigée en salle d’opération L’hypovolémie après évaluation
Statines
- Les statines doivent être continuées si elles étaient déjà en cours, et il semble y avoir un intérêt à les introduire en préopératoire en cas de chirurgie à haut risque (chirurgie vasculaire, etc.).
Inhibiteurs calciques
- L’arrêt la veille de l’intervention recommandé → potentialise l’effet vasodilatateur des anesthésiques
Digitaliques
- Durée d’action longue et marge thérapeutique très étroite. → favorise la survenue d’une toxicité (hypokaliémie, hypoxémie, etc.)
- L’ionogramme en préopératoire pour corriger surtout K+.
- Les taux plasmatiques préopératoires de digitaline doivent être contrôlés.
Antiagrégants
- Le plus souvent maintenus , surtout avec pathologie carotidienne ou une revascularisation coronarienne récente.
- Discussion entre cardiologue, anesthésiste et chirurgien.
Défibrillateur implantable, associé ou non à un pacemaker
- Possibilité d’interférence avec : le bistouri électrique (préférer un bistouri bipolaire, éloigner la plaque et éviter de situer le dispositif implanté dans l’arc électrique), mais aussi les fasciculations (succinylcholine), la radiofréquence, les potentiels évoqués, etc.
Période opératoire
Les mécanismes de compensation restent effectifs, mais ils sont altérés par l’effet des produits anesthésiques, durant cette période où la demande métabolique est faible lorsque la profondeur de l’anesthésie est adéquate.
Les facteurs de décompensation peropératoire sont essentiellement liés aux périodes de fortes variations hémodynamiques, qu’elles soient liées à l’anesthésie (induction, analgésie insuffisante) ou au geste chirurgical (hémorragie, clampage vasculaire, modifications hémodynamiques rapides)
Effets de l’anesthésie générale
- Permet une diminution de la consommation myocardique en O2, du fait de contraintes myocardiques moins importantes par baisse des conditions de charge.
- ↓de la réponse ∑ , une altération du baroréflexe, et ± une ↓ de l’inotropisme, de la conduction, et une action sur la vasomotricité modifiant les conditions de charge du ventricule.
- Le sevrage brutal de l’hyperactivité sympathique compensatrice lors de l’induction de l’anesthésie peut entraîner une chute brutale du débit cardiaque.
- À l’inverse, une stimulation nociceptive alors que l’anesthésie est insuffisante peut être délétère et mal tolérée par le biais de la stimulation ∑ et de l’élévation de la postcharge.
Médicaments de l’anesthésie
Induction
Benzodiazépines
- l’absence d’effet sur l’inotropisme , faibles effets hémodynamiques, augmentent la capacitance veineuse (chirurgie cardiaque +++)
Barbituriques
- Utilisables dans les insuffisances cardiaques compensées à condition de les titrer.
- Ils ont une action dépressive sur la contractilité.
Étomidate
- Permet le maintien relatif du tonus ∑ => Indiqué chez le patient insuffisant cardiaque.
- Effets cardiovasculaires sont quasi inexistants.
Propofol
- Utilisable avec prudence dans les insuffisances cardiaques compensées ;
- Peut être intéressant avec Rémifentanil en AIVOC
kétamine
- Provoque une stimulation sympathique et une vasodilatation.
- Place très restreinte (limitée à certaines chirurgies superficielles).
Morphiniques
- Pas d’effet inotrope,
- Ralentissent la FC (effet vagal),
- Action faible ou nulle sur la vasomotricité. Ils
- Sont utilisés à doses élevées pour limiter les conséquences de la stimulation nociceptive, et permettre de modérer les doses d’hypnotiques et leurs conséquences circulatoires.
Myorelaxants
- Action sur le SNA.
- Certains ont un effet vagolytique aboutissant à une augmentation modérée de la FC.
- L’atracurium possède un effet histaminolibérateur qui peut entraîner une hypotension mal tolérée s’il est injecté trop rapidement.
- La succinylcholine peut provoquer une augmentation transitoire de la FC, mais intéressant pour une induction en « séquence rapide ».
Entretien
L’utilisation des morphiniques en peropératoire doit permettre une atténuation des effets de la stimulation nociceptive.
Le niveau de myorelaxation dépend du geste chirurgical, et son monitorage est indispensable pour éviter une curarisation résiduelle très nuisible lors de la période de réveil.
Les anesthésiques volatils halogénés ont un effet inotrope négatif par action sur le calcium ionisé intracytoplasmique.
Le sévoflurane et le desflurane ont une action inotrope négative.
Cet effet est en partie compensé par la vasodilatation artérielle, diminuant la postcharge ventriculaire gauche.
Les variations rapides du taux inspiré de desflurane entraînent une stimulation sympathique qui doit être évitée.
Anesthésie locorégionale
L’anesthésie locorégionale médullaire entraîne une sympatholyse dans le territoire bloqué, associant une veinodilatation, une vasodilatation artérielle.
De plus, les anesthésies médullaires hautes inhibent la réponse sympathique myocardique, principalement impliquée dans les mécanismes compensatoires.
Les effets bénéfiques sont la diminution de la postcharge du VG dans le cadre des cardiomyopathies requérant une baisse de la postcharge, l’analgésie adaptée et persistant dans la période postopératoire immédiate.
Les risques sont en rapport avec
- Les variations rapides des conditions de charge ventriculaire pour les anesthésies médullaires,
- L’inhibition de la réponse myocardique à la stimulation sympathique,
- Les risques d’échec de la technique avec analgésie insuffisante et ses conséquences physiologiques.
- Toxicité cardiaque de la bupivacaïne
- Traitement anticoagulant ou antiagrégant plaquettaire avec anesthésies médullaires
Techniques doit être réservée à certaines situations où l’on attend un bénéfice par rapport à l’anesthésie générale, et nécessite un opérateur expérimenté.
Période du réveil anesthésique
La période du réveil est la période à risque chez le patient insuffisant cardiaque
Le réchauffement est le plus souvent nécessaire, quitte à retarder l’extubation, si l’hypothermie n’a pu être évitée en peropératoire.
Il doit être progressif, permettant d’étaler la récupération de la dette thermique.
Les facteurs d’augmentation de la demande en oxygène au réveil sont :
- frissons, qui peuvent multiplier par 3 ou 4 la consommation en oxygène ;
- sevrage de la ventilation assistée ;
- stimulation nociceptive.
Les modifications du retour veineux et l’absence de réserve myocardique (pour faire face à l’augmentation du débit cardiaque et la hausse de l’extraction tissulaire d’oxygène) expliquent la fréquence des décompensations, en particulier les œdèmes pulmonaires cardiogéniques.
La naloxone est contre-indiquée à ce stade.
Il faut faire attention à prévenir ou à corriger ces troubles :
- Normothermie ou sédation le temps du réchauffement ;
- Analgésie suffisante ;
- Sevrage de la ventilation une fois les autres paramètres corrigés,éventuellement sous traitement inotrope positif ;
- Contrôle de l’hématose (pression artérielle en oxygène [pao2], pression artérielle en gaz carbonique [paco2]) et correctiond’une anémie.
Date de dernière mise à jour : 21/09/2020
Ajouter un commentaire